编者按:
2020 年 9 月 21~22 日,热心肠研究院携手 Swisse 斯维诗于线上举办了 GUT2020 系列活动之“微生态营养补充剂与肠道健康前沿论坛”,特邀 8 位嘉宾出镜发表了在线演讲,共同探讨如何通过营养改善微生态环境,助力肠道健康。

今天,我们特别整理并发布同济大学附属上海市第十人民医院胃肠外科沈通一医生的演讲视频及图文实录,以飨读者。
沈通一
同济大学附属上海第十人民医院胃肠外科副主任医师
中华预防医学会微生态学分会青年委员
上海市预防医学会微生态专业委员会委员兼秘书
中华医学会肠内与肠外营养分会营养与微生态协作组成员


大家好,我是来自于上海第十人民医院胃肠外科的沈通一。我今天讲的是:治疗便秘,肠道微生态之路有几条?

因为我们知道便秘主要靠病史和相关的症状进行诊断的,它和别的疾病不一样,它没有相关的一些化验指标或者相关的病理诊断,所以很多人甚至于认为便秘它不是一种病,但是便秘的发病率却是非常高。

普通人群可以达到 16%,60 岁以上的人群,患病率可以达到 33%。
发病率高的原因首先一个就是很多人不重视,他出现了便秘,他也没有进行一个积极的治疗;第二种情况是传统的方法,它是没有效果的,所以导致累计的患者是非常高。
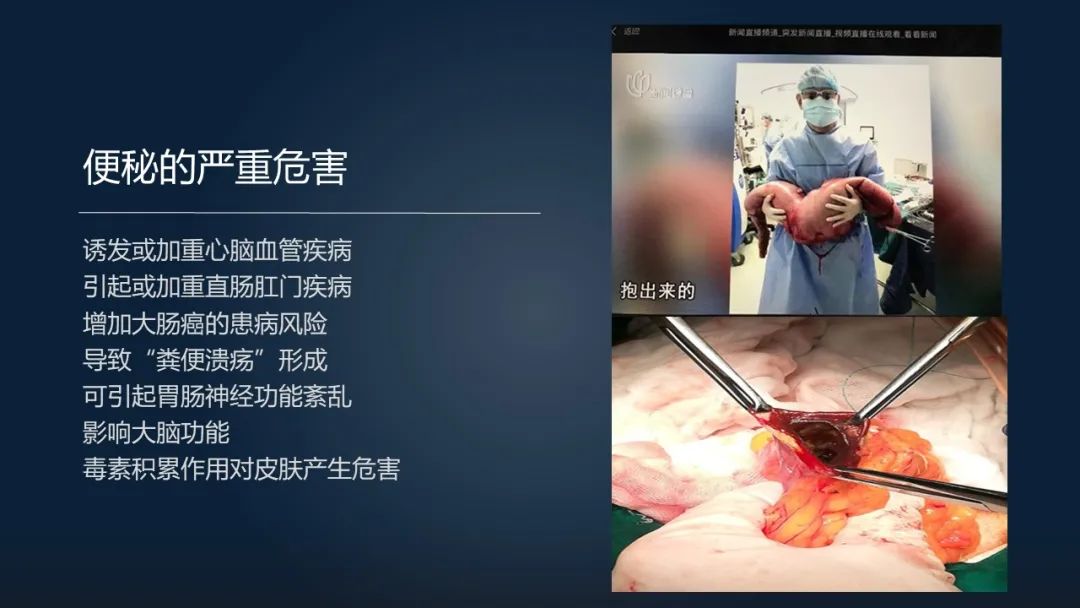
我们知道便秘它是个良性毛病,但它往往造成了非常严重的一个生活质量降低,比如说便秘它可以诱发或者加重心脑血管疾病,可以引起直肠肛门的相关疾病(比如说痔疮、肛裂等等),同时它还可以增加大肠的一个发病风险。
有很多人由于服用了大量的泻剂导致结肠发黑,同时由于神经的损伤也可以引起巨结肠。
便秘形成的原因有很多种,但现在最新研究其实发现肠道微生态它参与了便秘的发生和发展。
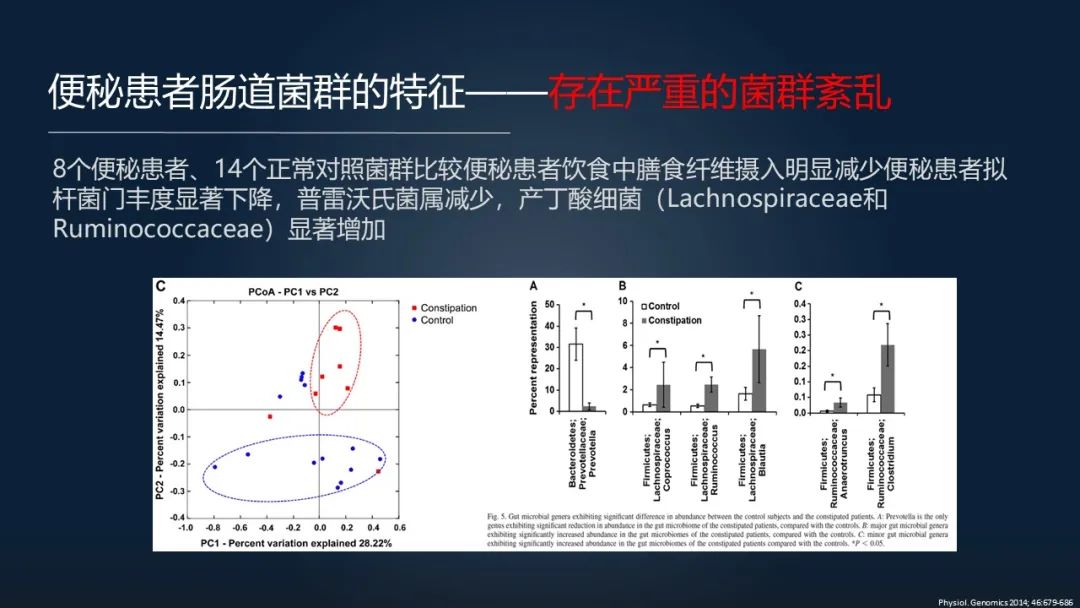
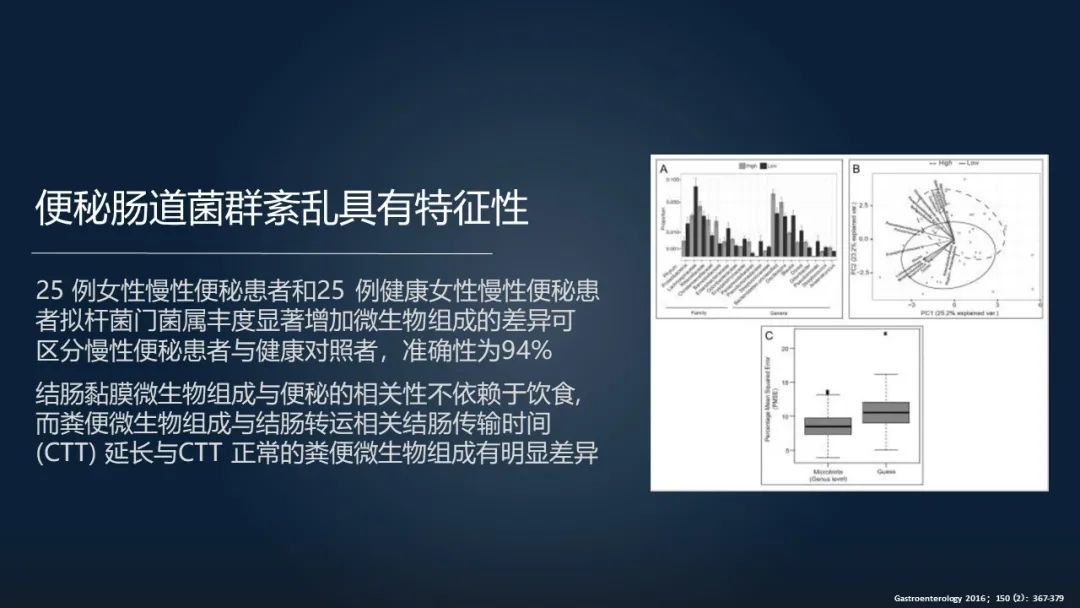
我们知道便秘患者有一个共同的肠道菌群特征,就是存在非常严重的菌群紊乱,甚至有人将这些菌群紊乱的特征用来判断一个人是不是便秘,准确率可以达到 94%。

便秘常见的症状包括大便变硬、排便周期延长以及排便次数多、排粪不尽感。
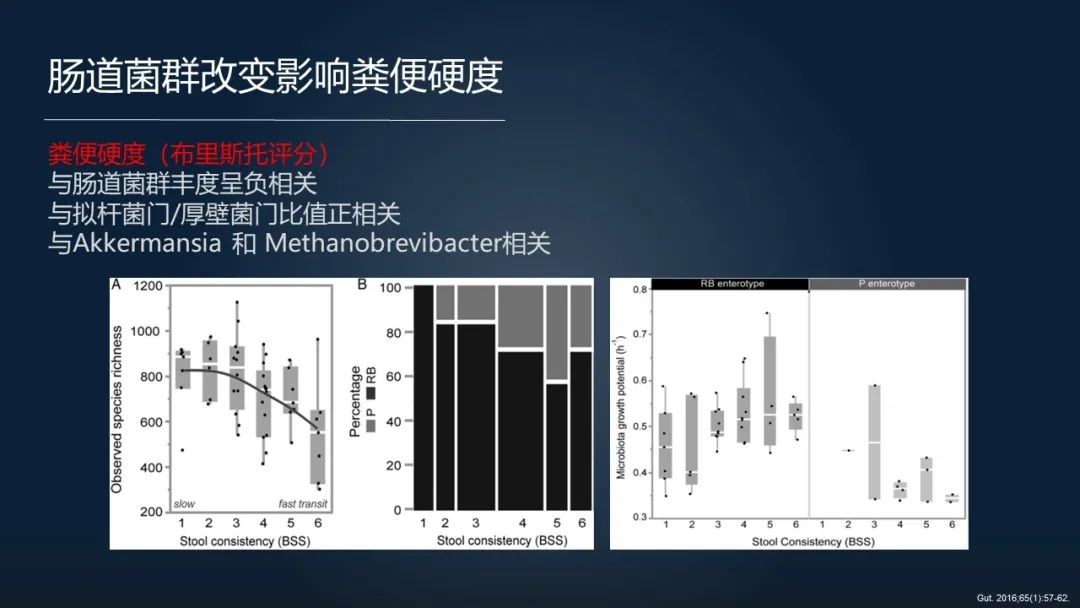
首先讲粪便硬度,研究发现粪便硬度和肠道菌群的丰度成负相关,就是说肠道的菌群数量越少,大便是越是硬。

而且有两项大型研究都发现了结肠菌群的组成和粪便的硬度是有关的。肠道菌群的改变引起粪便硬度改变的原因是什么呢?

其实我们肠道里面的粪便的组成,1/3 是菌,2/3 是食物残渣。我们往往依靠肠道菌群对食物残渣的发酵使大便变软,但是工作压力或者生活习惯不良都可以造成一个人肠道的菌群不足,而无法正常发酵可以导致我们的粪便变硬。
对于比较硬的粪便,我们可以看到粪便里面的纤维含量(包括膳食纤维的含量)越是多。

传统的观点认为,我们如果多服用一些蔬菜,或许便秘可以得到改善。结果很多人服用了大量的蔬菜,甚至于红薯,结果出现腹胀甚至于大便更加硬。
它的原因就是我们便秘患者本身的肠道菌群数量是不足的,他没有办法发酵,如果补充了过多的一些食物残渣或者含膳食纤维的一些食物,这点食物它没有办法正常的发酵以后,可以导致大便更加硬。
第二种观点就是说我们便秘是因为大便硬,我们才排不出来的,我们服用一些泻剂把过硬的粪便排掉,后面排便就不困难了。但是结果是我们在服用泻药的情况下,除了粪便被排出,正常的菌群也出现排出,造成菌群不足。一旦我们停用这些泻剂,排便以后大便会更加硬,出现一个恶性循环。
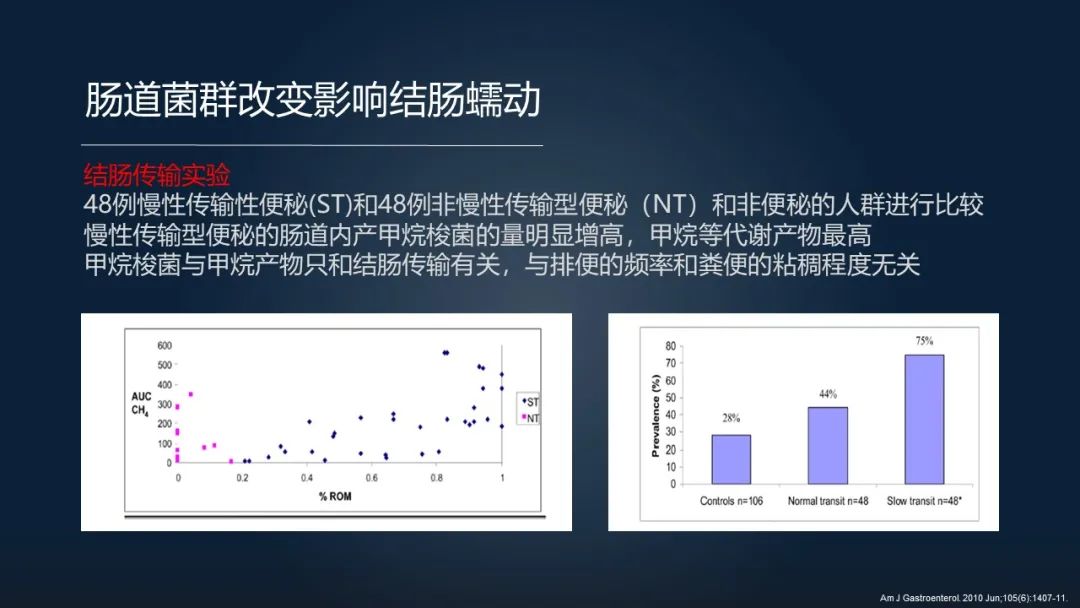
肠道菌群的改变它也会影响结肠蠕动。
比如说,现在发现慢性传输性便秘患者肠道内一些产甲烷的梭菌的含量是明显增高的,甲烷这些代谢产物也出现一个升高,而这些甲烷梭菌和甲烷代谢产物它只和结肠传输有关,它和排便的频率、粪便粘稠度是无关的。
这就说明了我们便秘它的根本原因往往不是一种菌造成的,它是多种菌共同作用的结果。
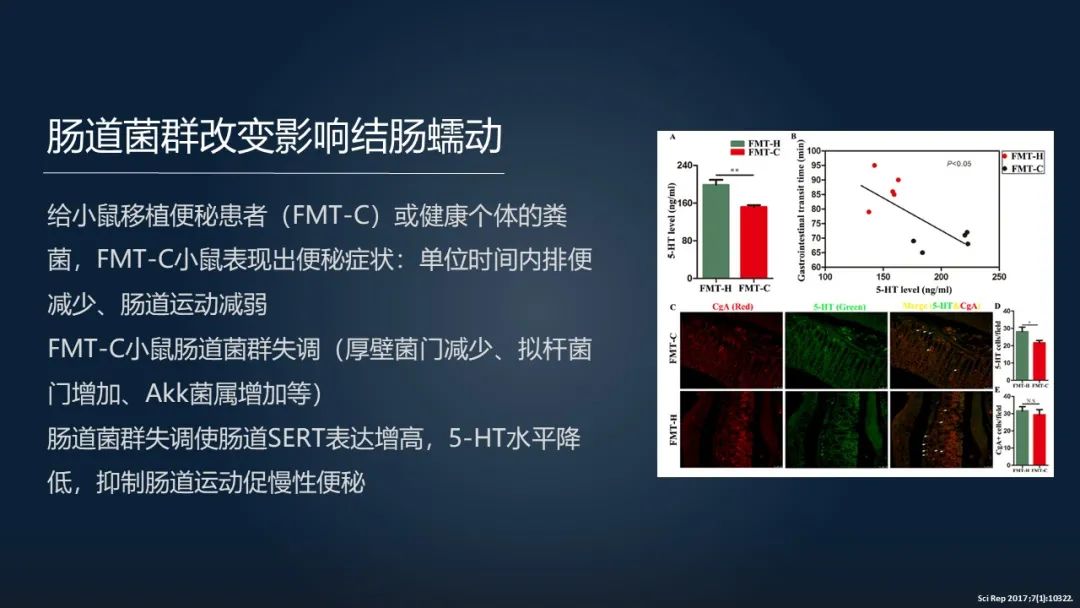
这里就是说有人给小鼠移植便秘患者的粪便,结果小鼠出现一些便秘的症状,包括短时间里面的它排便减少、肠道运动减弱,同时可以发现肠道菌群失调,肠道的五羟色胺水平降低,相关的转运体 SERT 表达增高。这些都可以抑制肠道运动,促进慢性便秘。
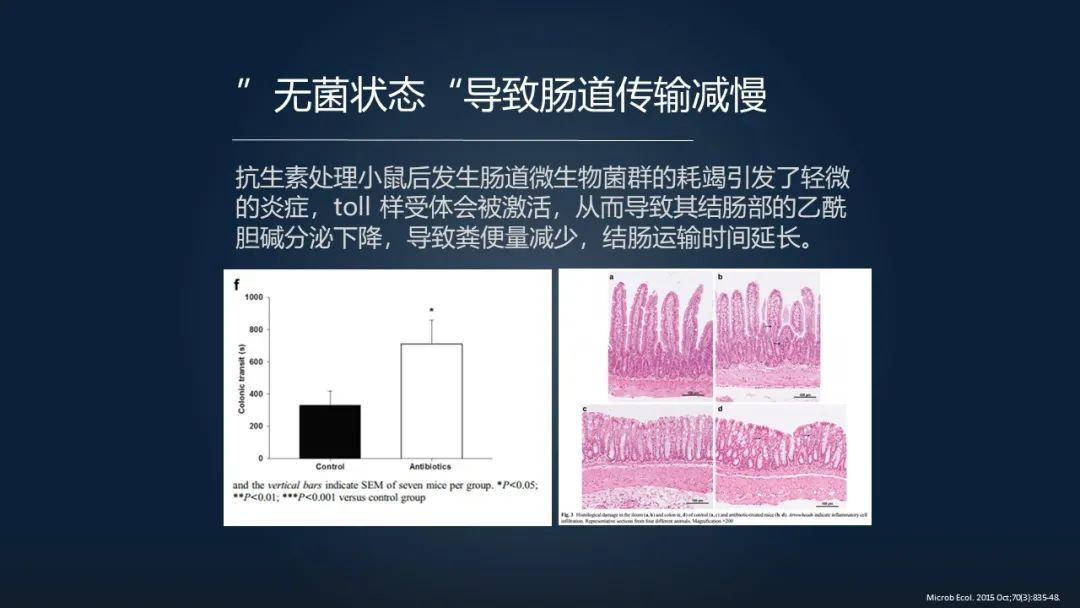
还有研究发现,在无菌状态下,无菌小鼠的肠道的传输是减慢的,我们在给小鼠使用大剂量抗生素以后,菌群的耗竭往往带来了一个 toll 样受体激活,导致粪便量减少以及结肠传输时间延长。

但是我们在给他补充了比较多的益生菌以后,发现就是高剂量益生菌补充和低剂量益生菌补充以及空白对照是不同的。
其中高剂量的益生菌补充,它的结肠传输时间缩短可以达到 28 个小时,低剂量它也可以缩短将近 18 个小时,但是空白组是没有明显的改善的。
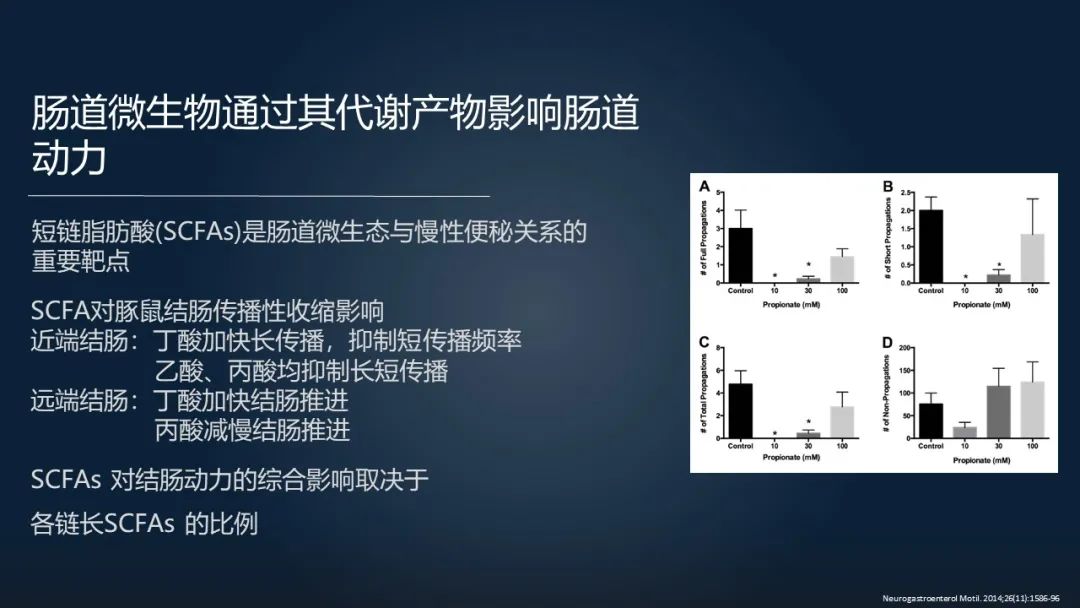
肠道微生物它主要是可以通过一个代谢产物影响肠道的动力,比如说短链脂肪酸。
短链脂肪酸在不同的结肠,在近端、远端,它不同的短链脂肪酸(包括丁酸、丙酸、乙酸)的比例不同,会影响到结肠传输的一个动力情况。
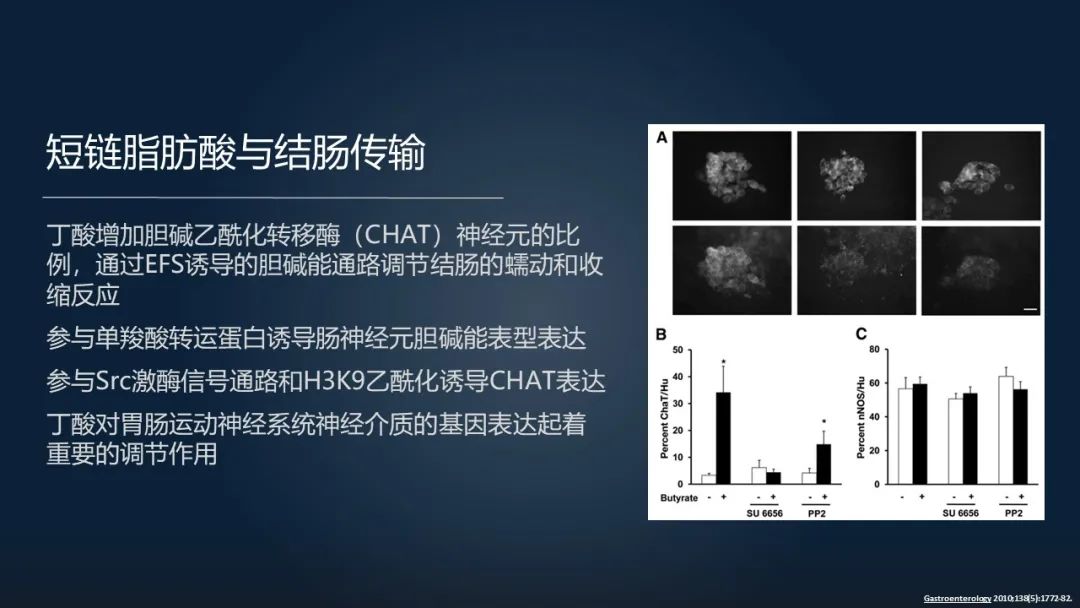
这篇研究发现就是说使用丁酸,我们可以增加胆碱乙酰化转移酶神经元比例,并通过诱导相关胆碱的通路可以调节结肠的蠕动和收缩反应。
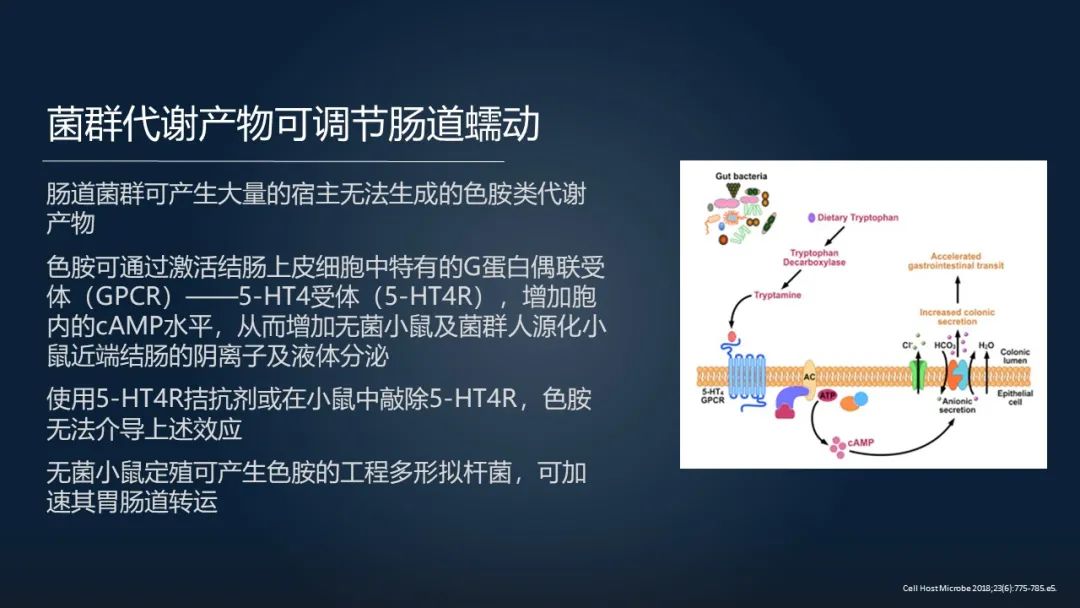
这篇文章发现,我们肠道菌群还可以产生大量宿主没有办法产生的色胺类代谢产物,包括五羟色胺。
而这些色胺可以通过激活结肠上皮的一种特有的相关的受体,包括五羟色胺受体,可以增加无菌小鼠以及菌群人源化小鼠的结肠里面的阴离子和液体的分泌。
通过相关的这些受体的拮抗剂可以阻断上述这些效应。

我们知道肠道的神经系统在肠道生理功能,比如肠蠕动中,其实发挥了重要作用。
在我们过去很长一段时间里面,我们都认为神经元作为永久细胞,可能是无法再生的,但现在研究发现,其实肠道神经系统一直在进行自主更新,并且通过神经干细胞凋亡来维持一个平衡。
而且还有研究发现,肠道微生物菌群它是出生后的小鼠肠道黏膜神经胶质细胞发育必须的。
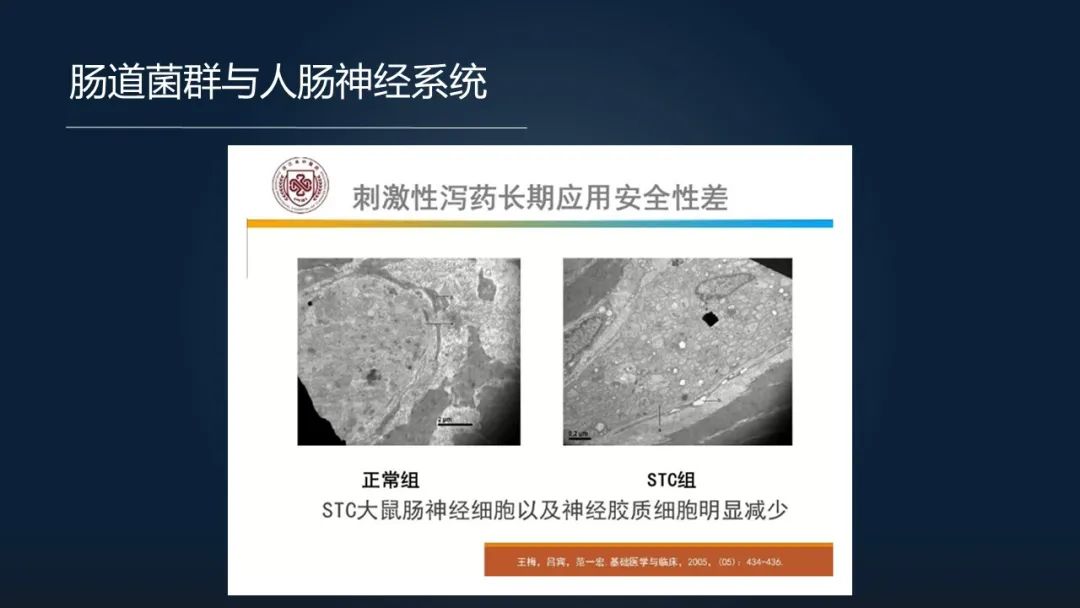
我们许多便秘患者他长期服用一些刺激性泻药,它会产生什么结果呢?
这是浙江中医药大学一位教授做的研究,给大鼠服用番泻叶等刺激性泻药以后,可以看到大鼠的肠神经细胞和神经胶质细胞出现明显减少。
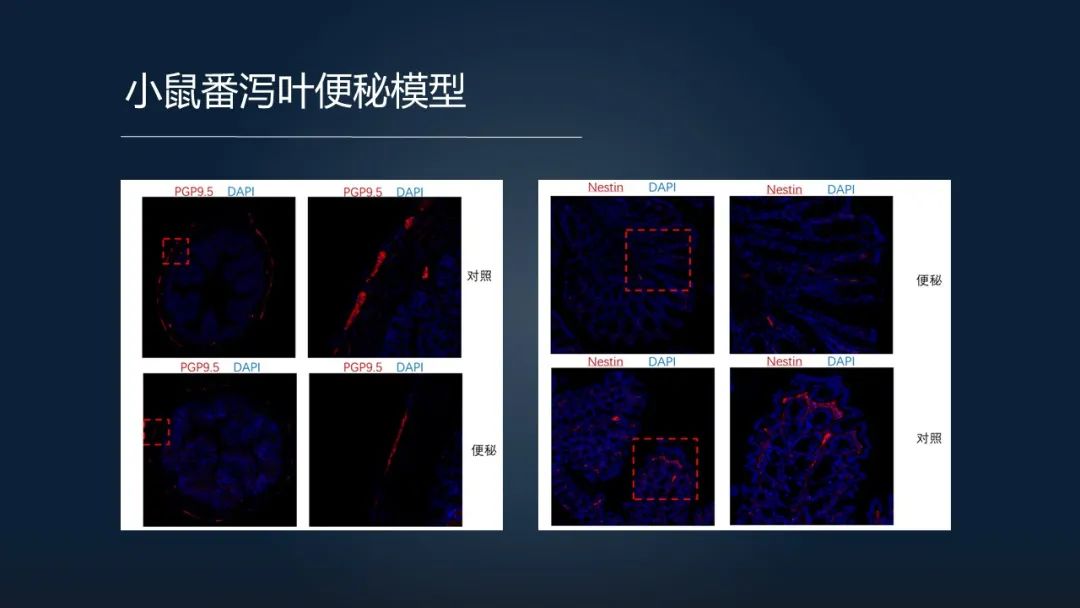
我们也和江南大学做了一个小鼠的番泻叶便秘模型。
左面我们可以看到便秘患者肠神经纤维出现明显的一个减少,右边我们可以看到这个相关的神经干细胞 NESTIN 小体,便秘组和对照组也出现了明显的一个差异。

同时我们对便秘患者和正常人的神经纤维做了个对比。我们将正常患者和长期服用泻剂的便秘患者他的肠道组织进行了对比,我们发现正常人的肠道上皮神经纤维染色可以发现有非常多的神经纤维,但是对于便秘患者他的神经纤维是明显减少的。
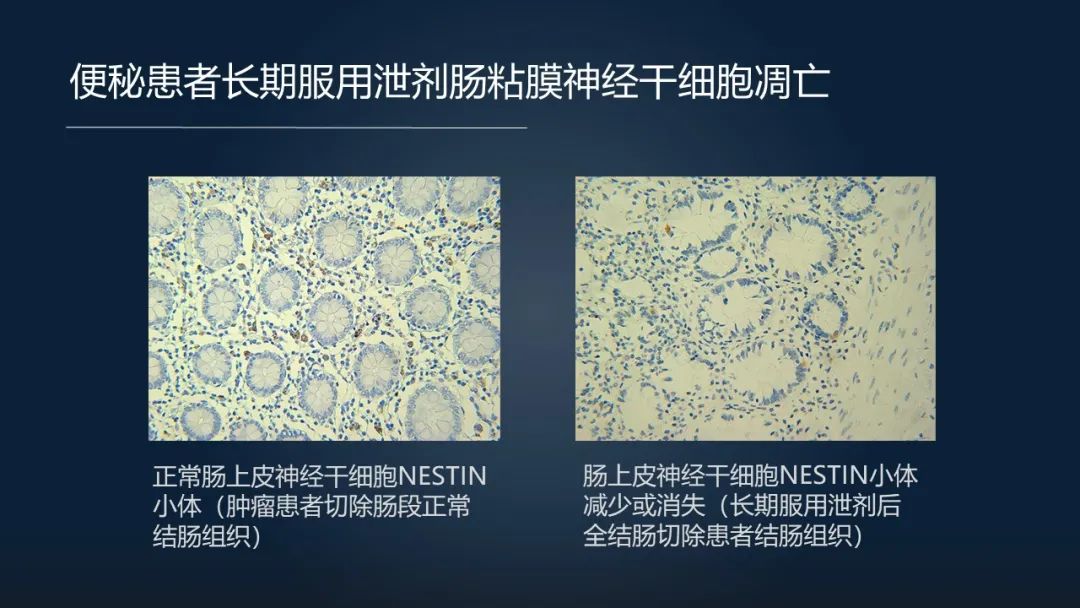
这里我们也可以看到正常的肠上皮里面神经干细胞 NESTIN 小体的分布是非常多的,而便秘患者肠上皮的神经干细胞的 NESTIN 小体是明显减少或者消失。
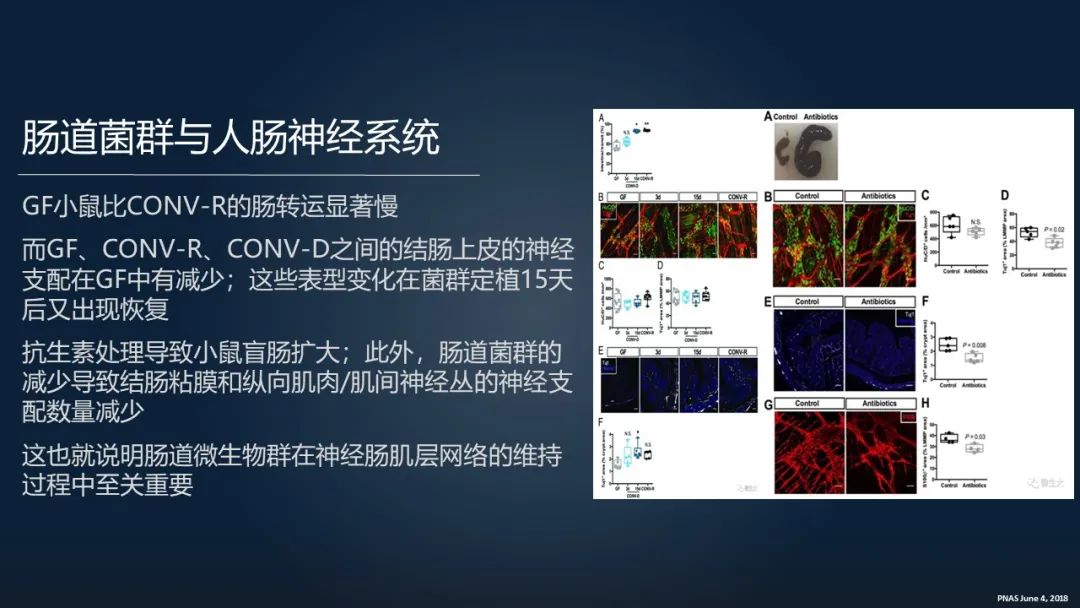
这篇文章是 2018 年 PNAS 上面的,他讲到了就无菌小鼠和正常小鼠相比,肠道的转运是明显减弱的。通过解剖上面对比可以发现,无菌小鼠肠粘膜上的神经纤维是明显减少的。
但我们将正常小鼠的粪便移植给这些无菌小鼠以后,在两个礼拜以后,这些无菌小鼠肠粘膜上皮的神经纤维出现了一个生长。
同时在我们用抗生素处理正常小鼠以后,我们可以看到这些小鼠的盲肠出现明显的扩张。同时我们可以通过解剖上面发现,它的结肠粘膜和肌间神经丛的神经的支配数量也出现明显减少。
这就说明了肠道微生物群在神经肠肌层网络维持中起到一个非常至关重要的作用。
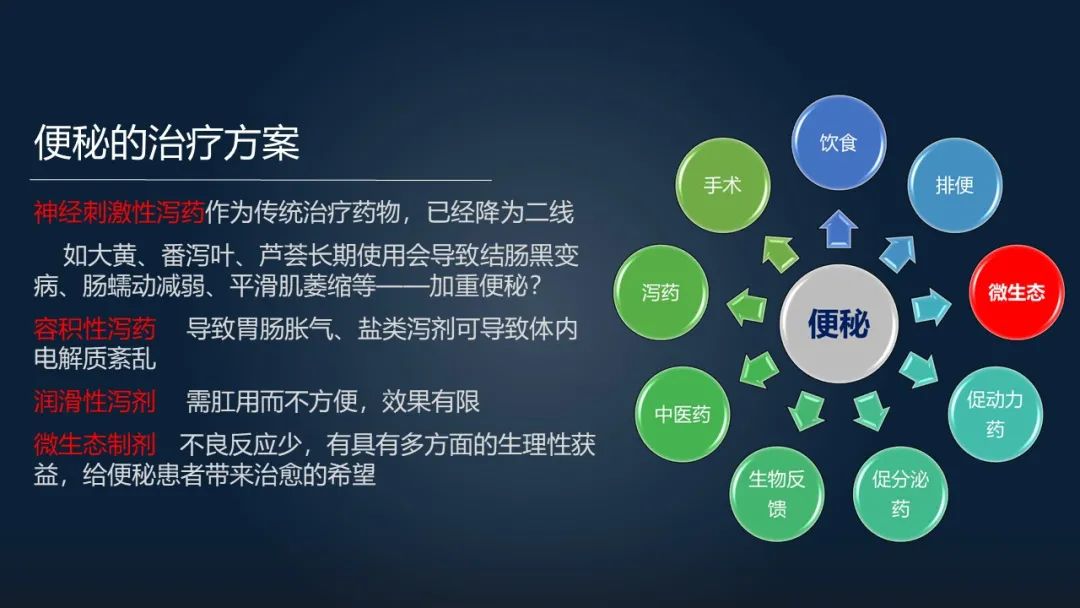
关于便秘的治疗方案,其实这是一个最糟糕的时代,它也是一个最好的时代。
因为我们发现传统的制药方案,包括无论是神经刺激性泻药,还是容积性泻剂,还是润滑性泻剂,它们只是对症治疗,没有办法根本来解决便秘的问题,甚至于在经过一段治疗以后,它可以出现效果逐步地降低的情况。
而这也是一个最好的时代。因为我们发现肠道微生态制剂它不仅不良反应小,而且具有多方面的生理性获益,给我们便秘患者带来了一个治愈的希望。

这是 2016 年的《便秘外科诊治指南》,它已经提出了经过口服肠道微生态制剂调节肠道微生态平衡对缓解便秘和腹胀起到了一定的作用,但是我们要进一步明确微生态治疗在便秘治疗中的一个重要作用。

这是 2016 年欧洲的便秘的治疗指南。当中提出了益生菌已经被确认在大便相关疾病,包括在功能性便秘的一个正常的过程中其发挥的作用。
尽管这些产品中的大多数只能作为一种食品补充剂开发,但它们有潜力作为医药产品开发。

说到便秘微生态治疗,首先我们都会想到粪菌移植,确实粪菌移植可以将健康人的粪便中的一个功能菌群移植到患者胃肠道内,同时重建具有正常功能的肠道菌群,实现肠道与肠道外疾病的一个诊疗。

2017 年的时候,李宁教授来到我们医院给我们带来了粪菌移植和粪菌胶囊。

他的研究对 24 例慢性传输型便秘患者随访了 12 周,临床改善率达到 65%,而 12 周后,患者的粪便性状评分、结肠传输时间和每周排便次数以及便秘评分均有明显改善,没有看到明显的不良反应。
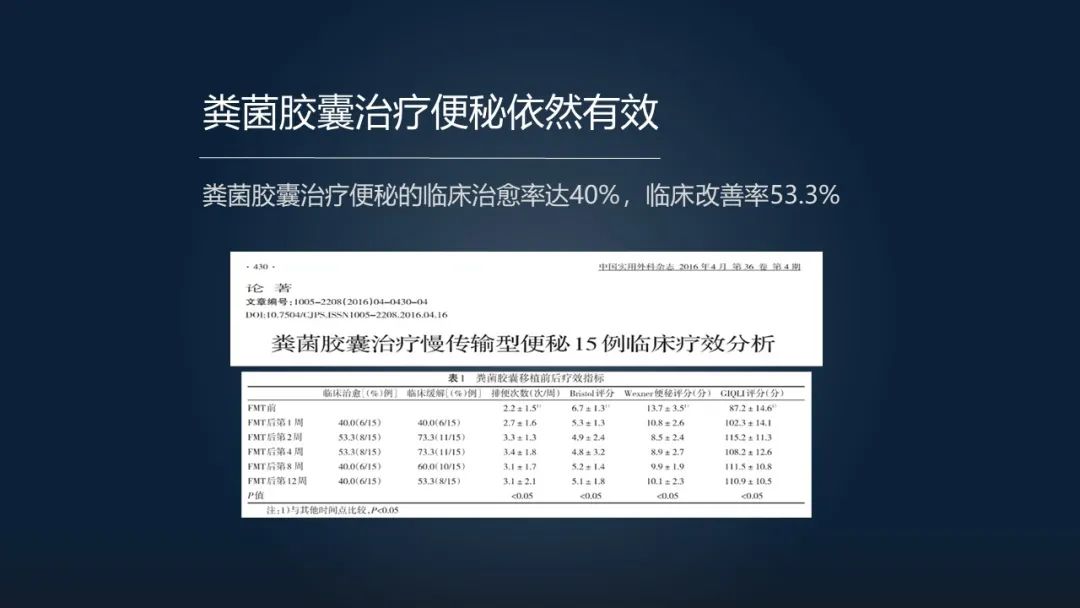
通过粪菌胶囊治疗便秘,它临床治愈率也达到 40%,它的临床改善率可以达到 53.3%。

但是关于粪菌移植,它也有很多争议的问题。
首先这篇关于如何优化粪菌移植的文章里面,他就提出了由于肠道微生物它的复杂性和每个人的个体差异,导致粪菌移植的作用、机制目前还没法明确。同时,他也提出没有通用的超级粪便,不是所有的毛病都可以通过粪菌移植来解决。

这是张发明教授。他提出了由于粪菌里面有有益菌,也有有害菌,所以他认为粪菌移植的未来是一些配方的菌群移植,甚至于迷你粪菌移植。就是说我们可能不需要这么多菌,而是根据每个病人的需要进行一个配方的菌群移植。

这是 2017 年的《柳叶刀》的一篇综述。这篇综述里面它最后提到的一个观点就是说粪菌移植的终极目标是无需供体。什么叫无需供体?就是一个个性化、标准化的细菌组合。人工粪菌或许才是一个终极解决的方案。
比如说,我们可以建立一个粪菌银行,根据每个人的情况进行个体化的一个治疗。

当然,我们也要重视粪菌移植的风险。
去年有报道两例粪菌移植,治疗复发性艰难梭菌感染以后,发生了产气荚膜梭菌感染,病原菌就可能来自于粪菌个体。
FDA 也报道了美国两名免疫受损的成年患者进行粪菌移植后,由于相关的耐药菌的感染,导致其中一人死亡。而且 FDA 正在停止一系列的粪菌移植临床试验,直到他们制定了相关的一个程序来筛选捐赠粪便中的一个危险微生物。

这是去年 Martin J Blaser 在《新英格兰杂志》上面发了一篇文章,他提出要正确认识粪菌移植带来的风险。
他提出了就是说虽然经过筛选,肯定会降低已知感染的风险,但是有很多新的一些病原体,比如说当初的丙型肝炎病毒、人类免疫缺陷病毒等等,直到这些新的病原体被移植到宿主后,我们才发现它们,所以我们很难确定一个具体风险源。
所以他最后提出了要重视研发有针对性的益生菌组合或者益生元,以及考虑使用噬菌体来治疗的一种可行性。

我们知道由于新冠的影响,不光是美国,中国大陆地区的粪菌移植的数量都受到了影响。因此,全球有 10 个国家将组织 25 名专家于近期联合制定相关的医学指南,其中他们对粪菌移植的安全性,无论是筛选排查,还是相关实验室设备等都提出了一些更高的要求。

这是 2018 年 Cell 上的一篇文章。有人提出了未来趋势是进行个性化的益生菌干预,但是使用益生菌要定植在肠道也受到很多因素的影响,包括我们宿主的基因、不同肠道的原籍菌,它的个体化差异是巨大的。而且,在干预前的宿主的菌群特征可以预测益生菌的肠道粘膜定植的效果。

我们在 2016 年在十院成立了肠道微生态临床研究和诊治中心。

这是 2016 年到 2017 年的时候,我们选取了 373 例慢性便秘患者,我们给予的是五株 300 亿的益生菌结合聚乙二醇 4000 散。
在使用三个月以后,它的有效率可以达到 50%。但我们发现如果在单独使用益生菌的情况下,它的有效率仅仅在 30%左右。它治疗有效多集中在便秘时间比较短、不使用泻剂人群,而无效集中在长期服用芦荟、番泻叶等药物的人群。

从 2018 年开始,我们增加了益生菌的制剂的剂量。
我们随访了 2018 年到 2019 年的 873 例的便秘患者,我们发现同时结合聚乙二醇或者乳果糖使用,可以使整体的有效率上升到 70%以上。
而且我们根据治疗前后的一个代谢组的结果,通过数据分析建立了便秘的预后治疗方案的预测模型。我们希望在新的人群里面可以进一步验证。
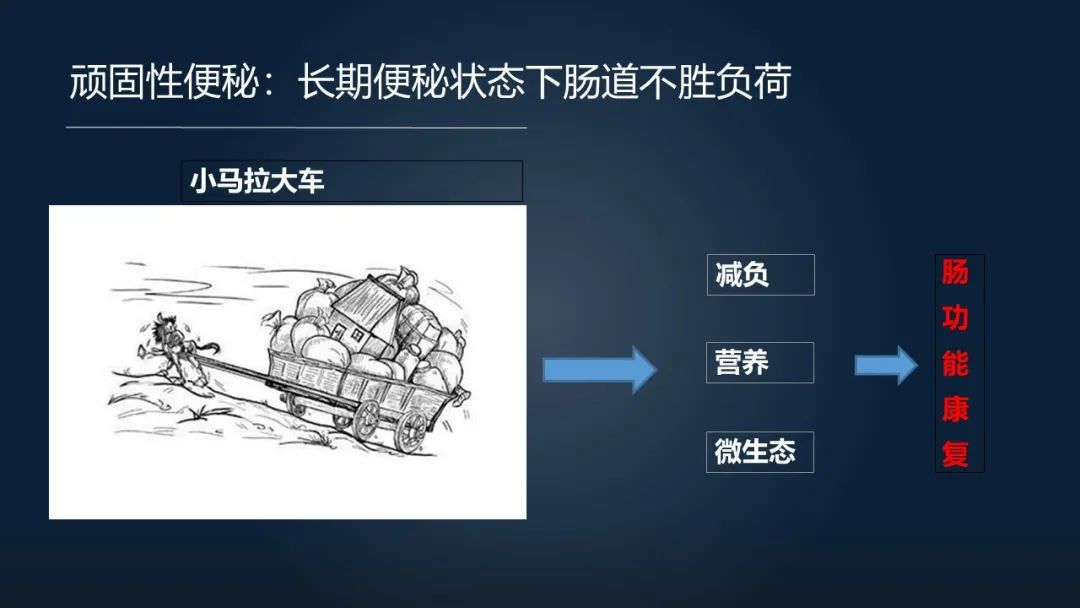
我们知道顽固性便秘患者他由于长期服用泻剂会导致肠道菌群紊乱,同时肠道神经受到损伤。在正常饮食的情况下,大量的食物残渣或者粪便堆积在肠道内,肠道就和小马拉大车一样,负担很重,而且一直得不到休息。
这种情况下对我们肠功能恢复会产生很大影响,所以对于这种情况,我们建议是要及时进行减负。打比方我们吃的东西尽量消化,甚至于我们服用流质,服用流质饮食来减轻肠道的负担,让肠道得到充分的休息。
同时我们要给它营养支持以及补充足够的肠道微生态制剂,让肠道的菌群进行恢复的同时,让神经也得到修复,这样就可以有利于肠功能的早日康复。

这里有篇文章就提出了每天摄入 70 亿或者 700 亿的一个肠道微生态制剂,持续两周,发现较高菌数和多菌种益生菌制剂往往可以带来更早和更高程度的一个菌群恢复。
同时,肠道菌群密度也成为现在当前新的一个研究方向,肠道菌群密度和宿主之间的关系往往有助于推进肠道菌群在疾病的预防和治疗当中的应用。

根据粪菌移植的方法,我们专门设计了益生菌的菌群植入。
我们在第 1 天给患者进行一个肠道造影;在第 2~5 天留置胃管,给患者输入肠内营养以及服用大剂量益生菌,每天在 8000 亿的菌量;在第 6~10 天,我们在拔除胃管的同时,将益生菌的菌量逐步减少;在第11天出院。

这是我们在 2018 年开始进行的首批的益生菌菌群植入患者。这些患者有老人,有年轻人,有门诊治疗失败的患者,有粪菌移植失败的患者,有手术失败的患者。
我们每天给他们 10 株益生菌,大概是 8000 亿的菌量的植入。
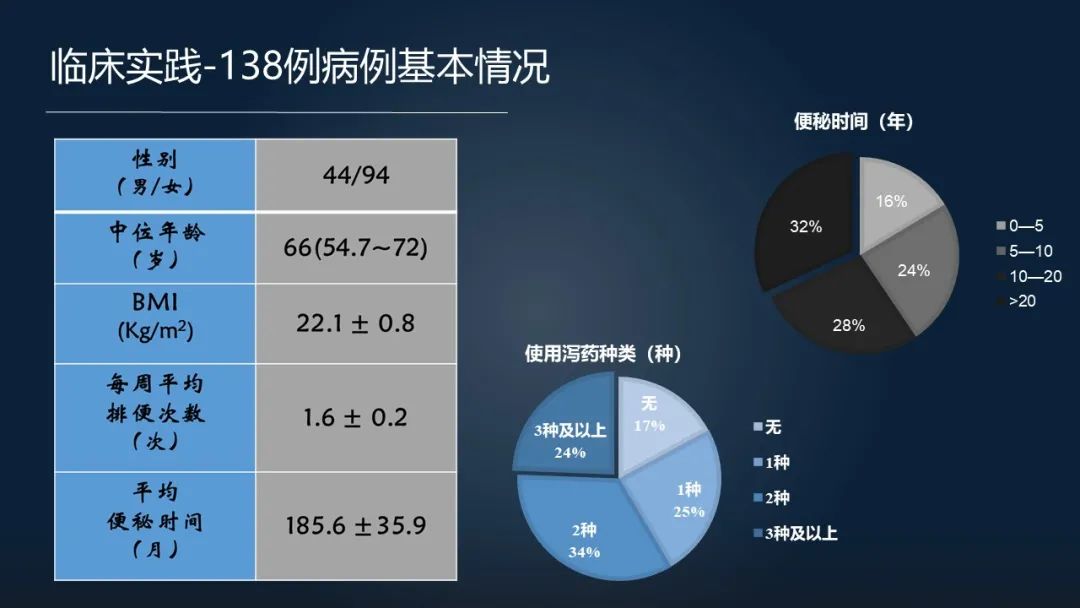
住院患者总共 138 例,平均的每周排便次数在 1.6 次,平均的便秘时间在 15 年以上。
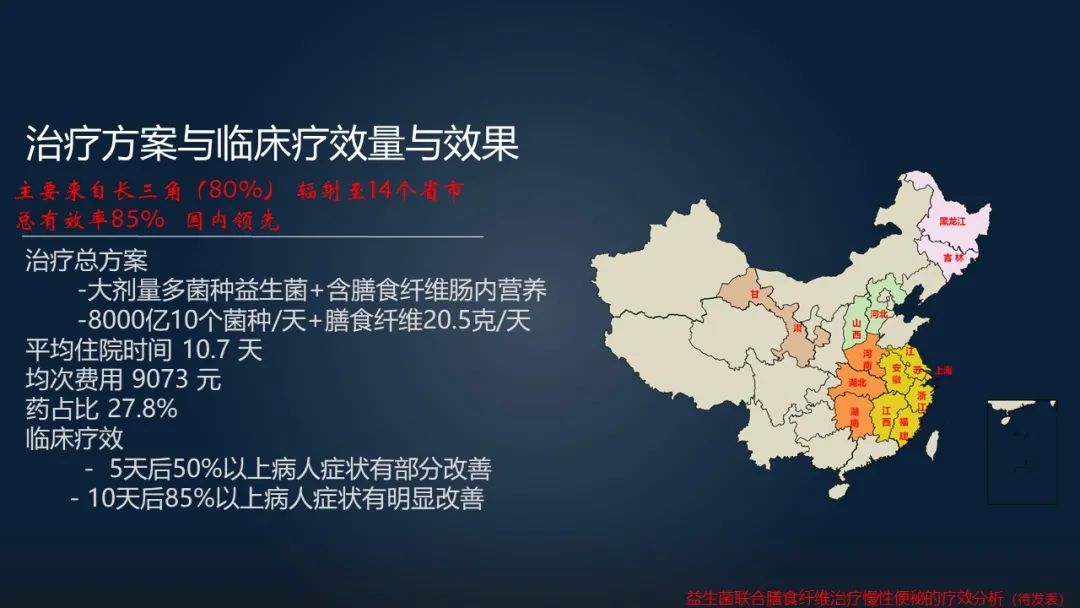
根据临床疗效,我们看到在 5 天后,50%以上的病人,他症状有部分改善。在 10 天以后,有 85%以上的病人,他的症状是出现了一个明显的改善。

根据益生菌移植疗法的一个特点,我们归纳了一下它的优点是:它的治疗过程是简便的,病人他依从性高,安全性高,容易推广,而且短期疗效是非常显著的。
但它也存在不足之处:它没有大样本的数据,它也无法反映真实疗效;第二个就是说,它的菌种菌量和粪菌移植比还是存在不足,目前还不能达到一个个性化治疗;而且它也没有办法阐明它的作用机制。
但是我们相信益生菌移植疗法它有希望和粪菌移植在便秘治疗领域相互补充。
最后我要讲一下,我们知道便秘的发病率很高,但目前相关研究是明显不足的。
另外,我们要如何纠正便秘患者对治疗手段的传统认识?比如说我出现便秘并不是急着去吃一些泻药,我们可以服用一些肠道微生态制剂,或许它有助于提高便秘治疗的一个整体疗效。
还有就是如何针对患者肠道的实际情况,我们来定制一些个体化的治疗,或者我们开发一些靶向性的微生物药物,这是将来我们需要做的一件事情。
最后就是说,以菌为药,从治疗到治愈,微生态制剂治疗便秘还是有广阔的研究和应用空间。

谢谢!



