
编者按:
2021 年 1 月,推特(Twitter)上举办了一场名为“将你的科学‘艺术化’,科学家如何用艺术来表达他们的工作(Art-ifying Your Science, How Scientist Can and Do Use Art to Communicate Their Work)”的线上会议。有不少科学家用生动的画笔描绘了那些晦涩难懂的科学机理。
今天,我们特别分享这次活动中与微生物有关的作品,并对相关的科学概念做简要介绍。同时,也预祝诸位读者新年快乐!
微生物的群体感应(quorum sensing,QS)是微生物间化学通信的过程,广泛存在于各种微生物中。这种信号交流机制,依赖于细胞外信号分子的产生、分泌、检测和响应,用以监测菌群密度、调控菌群生理功能,并且能够显示出少量菌体或单个菌体所不具备的特征1。
群体感应又被称为“细胞与细胞的交流”或“自诱导”。参与这一过程的关键信号分子,则被称为自诱导分子。随着微生物不断生长,群体密度及自诱导分子浓度到达一定阈值时,就会启动微生物特定基因的表达,以协调或调控微生物的生物功能。
图片来源:https://twitter.com/NoemieMatthey/status/1352648932090904576/photo/1
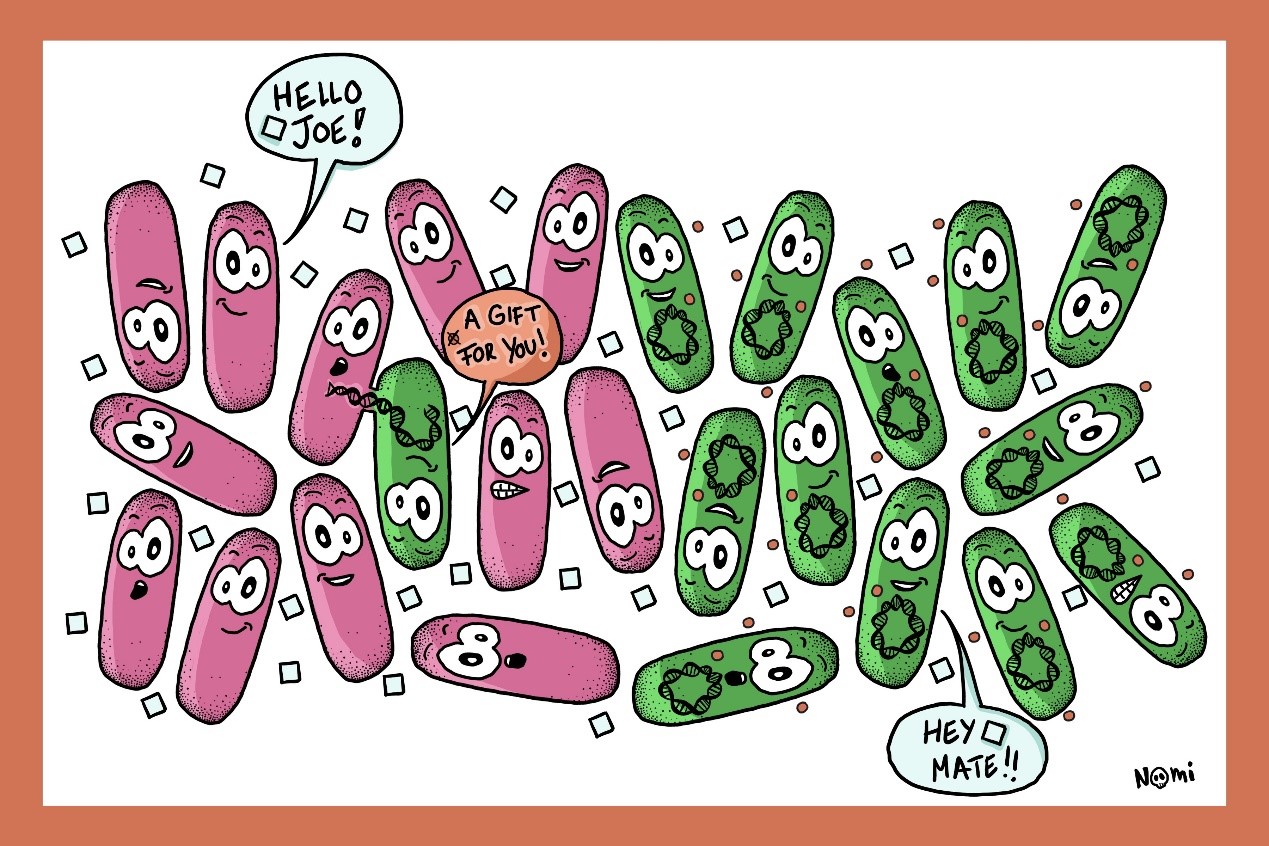
Noémie Matthey(@NoemieMatthey)所绘制的这幅图正是描绘了两种枯草芽孢杆菌间形成的群体感应。两种枯草芽孢杆菌通过分泌不同的自诱导分子(图中用白色方形和橙色小圆点表示),来对自己的群体行为进行调控。
此外,作者也在这幅作品中体现了微生物的基因水平转移(HGT)机制。当两种枯草芽孢杆菌“相处”的时间长久了之后,感情日益增进,在偶然的一天里,可能就会有其中一种枯草芽孢杆菌满怀期待地,送给对方一段 DNA 序列作为礼物,从而实现细菌之间的基因交换,促进细菌进化。
在漫长的进化历程中,细菌进化出了多种信号转导机制,来响应外界刺激(输入),产生不同的反应(输出)。化学感应(Chemosensory)途径在细菌中广泛存在,是最复杂的信号机制之一,需要多种蛋白质的参与。
在这一途径中,细菌外的信号分子与细菌表面的化学感受器结合,以激活下游的反应2。而这个概念又引发了不少科研人员的奇思妙想……

图片来源:https://twitter.com/she_toot/status/1352945682227859457/photo/1
在日常生活中,我们会用开瓶器来打开啤酒瓶的盖子,而在没有开瓶器的时候,我们则会找一些类似的物件来替代开瓶器,比如钥匙、勺子等等。
由上可知,如果想要启动细菌的化学感应途径,就需要一种与化学感受器相匹配的信号分子,那么,在缺少这种信号分子的情况下,结构相似的信号分子,是否也能起到类似的化学感应作用呢?
Shraddha Shitut(@she_toot)创作的这幅画给了我们答案。她将细菌比作了啤酒瓶,而我们也有多种方式可以启动细菌的化学感应途径。
图片来源:https://twitter.com/fsantoriello/status/1352668711166074881/photo/1
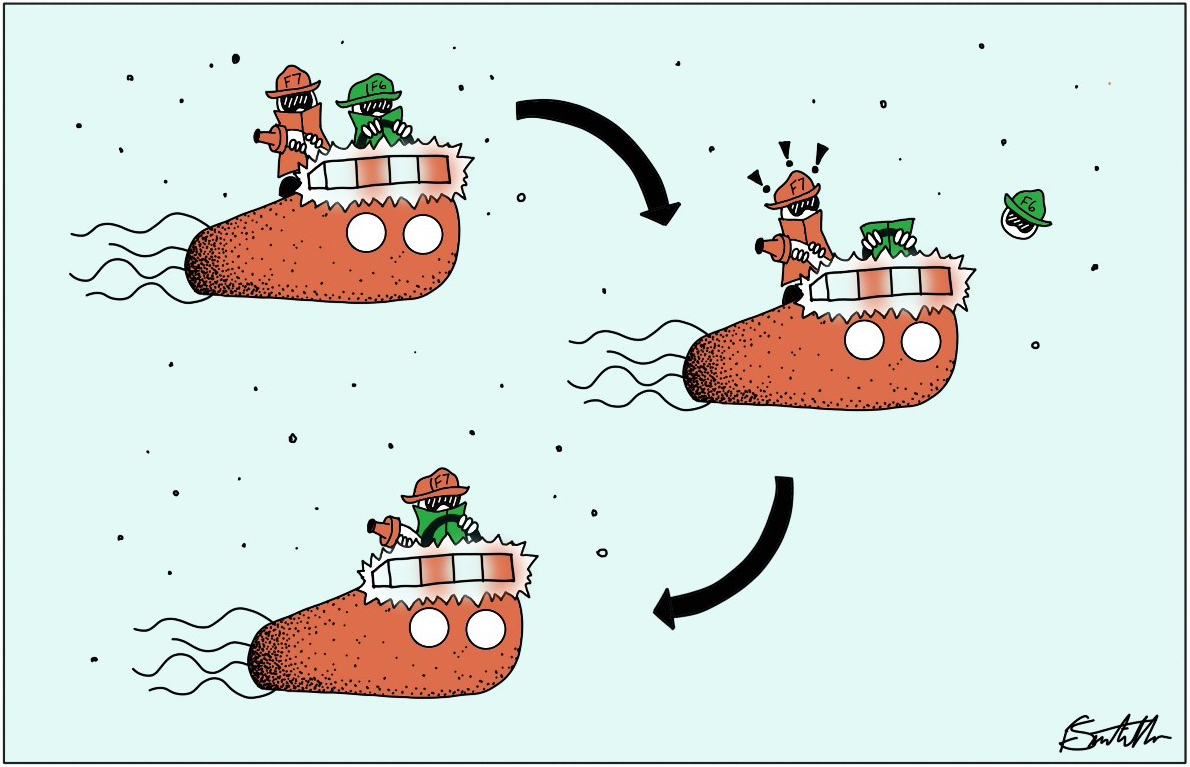
2020 年的一项研究对控制大肠杆菌鞭毛运动的化学感应机制进行了探索,发现大肠杆菌细胞内存在两套不同输入和输出的化学感应系统(γ-变形菌门的 F6 系统和大肠杆菌科的 F7 系统),而且 F7 系统可以接管 F6 系统的输入和输出,最终导致 F6 系统丢失3。
Frank Santoriello(@fsantoriello)绘制的这幅图生动地说明了上面这项研究的结果,F6、F7 两位“驾驶员”的遭遇,不仅体现出大肠杆菌内化学感应系统的变化,也阐明了 F7 和 F6 两套化学感应系统与鞭毛协同进化的过程。
沙门氏菌被巨噬细胞吞噬后,会先驻留在巨噬细胞内的酸性囊泡中。这样的酸性环境可以让沙门氏菌的细胞质酸化,当酸化至 pH=5.6 时,沙门氏菌中的 SsrB 蛋白会磷酸化、活化,从而与 DNA 进行结合,促进沙门氏菌致病岛 SPI-2(pathogenicity island 2)基因的表达4。
SPI-2 大量表达,使得沙门氏菌的毒力大增,三下五除二就杀死了吞噬自己的巨噬细胞,这种“遇酸则强”的防御能力,是沙门氏菌在长时间的进化中演变而来的。
相反,当 pH 逐渐升高至中性或碱性时,SsrB 蛋白就无法大量活化,也无法大量表达 SPI-2,最终只能束手就擒,被机体的免疫系统所消灭。
Noémie Matthey(@NoemieMatthey)绘制的这幅图,为我们很好地解释了这样一个繁琐的机制,也提示我们,碱性环境更利于杀死沙门氏菌。

图片来源:https://twitter.com/NoemieMatthey/status/1351590991833268227/photo/1
蛭弧菌(Bdellovibrio bacteriovorus)是一种可以寄生于其他细菌(也可无寄主而生存)并能导致其裂解的细菌。蛭弧菌属于革兰氏阴性菌,比一般的细菌要小,并具有类似噬菌体的作用5。

图片来源:https://twitter.com/NoemieMatthey/status/1352652553117442048/photo/1
近年来,抗生素的大量使用,使得多重耐药(multi-drug resistant,MDR)菌成为一个棘手的难题。因为蛭弧菌具有类似噬菌体的功能,能够裂解许多抗生素无法攻克的致病菌,所以近年来许多学者将目光转向了蛭弧菌。
Noémie Matthey(@NoemieMatthey)绘制的这幅作品为我们呈现了这类特殊细菌对耐药菌的杀伤力。
外排泵(efflux pumps)是细菌将胞内的药物或毒性物质排出胞外的蛋白转运系统,在外排过程中,需要进行质子交换或水解 ATP 提供能量。这种外排泵系统也可以将抗生素排出细菌外,是临床上固有耐药和获得性多重耐药的主要机制6。
然而“道高一尺,魔高一丈”,有一种名为“χ-噬菌体”的噬菌体,可以沿着鞭毛丝随机吸附,然后利用这些外排泵,将它们的遗传物质注入沙氏门菌的细胞中,从而杀死细菌7。
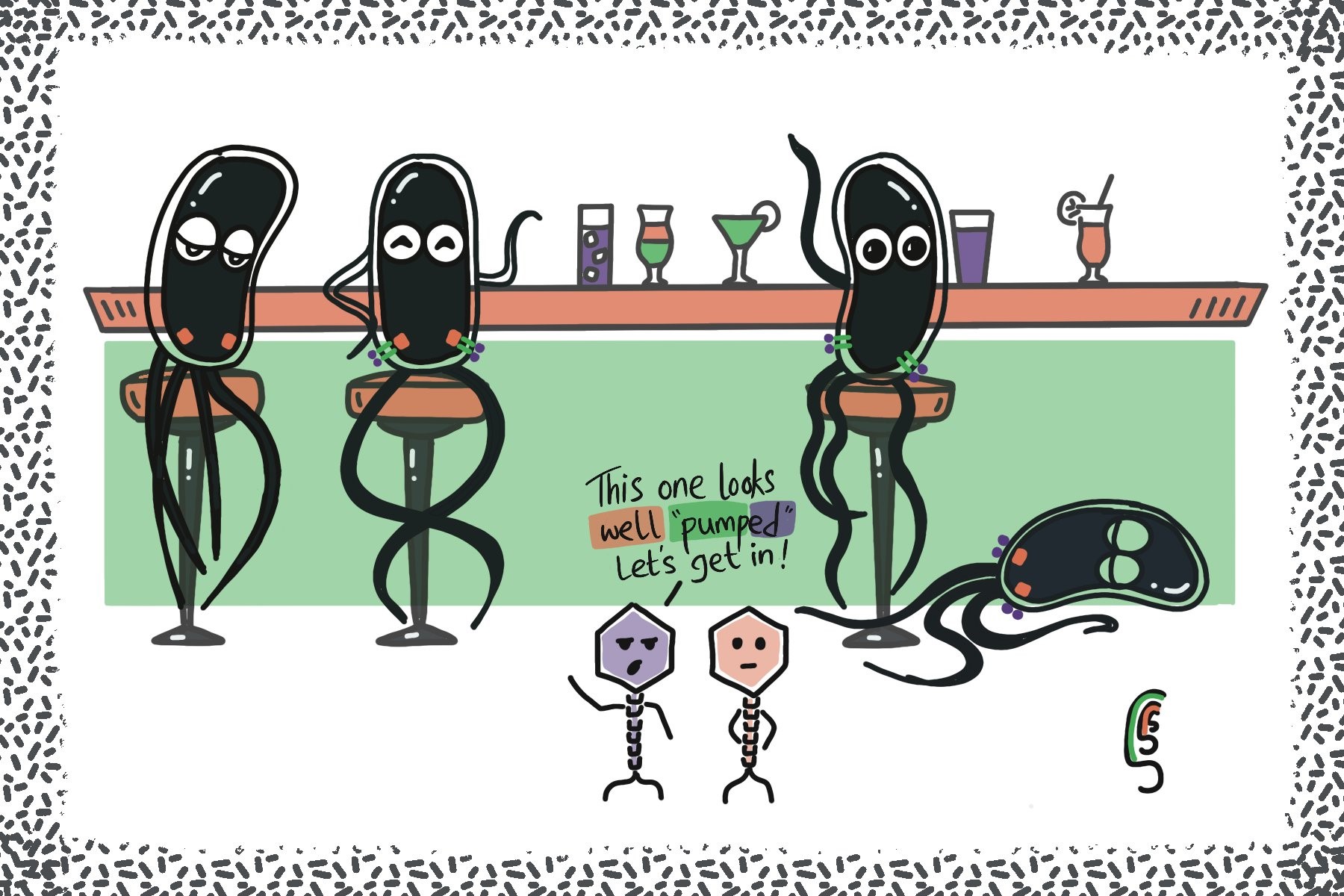
图片来源:https://twitter.com/she_toot/status/1352336342139740161/photo/1
在 Shraddha Shitut(@she_toot)绘制的这幅作品中一位倒在地上不胜酒力的沙门氏菌,就成了 χ-噬菌体的猎物,因为它既有鞭毛,又有外排泵,恰恰符合 χ-噬菌体的条件。
新月柄杆菌(Caulobacter crescentus)是一种无毒的单细胞生物,属于 α-变形菌纲,革兰氏染色阴性。这种细菌生活在养分很少的水生环境中,如河流、湖泊和海洋。
新月柄杆菌最大的特点是,单个细胞可形成两种不同类型的细胞:当它们需要寻找养分的时候,它们会化成可游动的细胞,以探索环境、寻找资源;当它们需要产生后代,进行复制分裂的时候,它们会变成一种不可游动的叶柄状细胞8。
这一特点引起了科研人员的兴趣,因为新月柄杆菌可以作为一个简单而又便捷的单细胞模型,来研究细胞分化、非对称分裂以及它们与细胞周期进程的协调关系。

图片来源:https://twitter.com/NoemieMatthey/status/1351987160858185730/photo/1
在上面这幅图中,Noémie Matthey(@NoemieMatthey)用可爱的笔调,画出了新月柄杆菌的两种形态,再搭配上精细的表情,让观者对新月柄杆菌过目不忘。
参考文献:
1.Mukherjee S and BL Bossier. (2019). Bacterial quorum sensing in complex and dynamically changing environments. Nature Reviews Microbiology 17:371-382.
2.Matilla M, D Martín-Mora, J Gavira, TJM Krell and mbr MMBR. (2021). Pseudomonas aeruginosa as a Model To Study Chemosensory Pathway Signaling. 85.
3.Ortega DR, W Yang, P Subramanian, P Mann, A Kjaer, SY Chen, KJ Watts, S Pirbadian, DA Collins, R Kooger, MG Kalyuzhnaya, S Ringgaard, A Briegel and GJ Jensen. (2020). Repurposing a chemosensory macromolecular machine. Nature Communications 11.
4.Liew ATF, YH Foo, YF Gao, P Zangoui, MK Singh, R Gulvady and LJ Kenney. (2019). Single cell, super-resolution imaging reveals an acid pH-dependent conformational switch in SsrB regulates SPI-2. Elife 8.
5.蔡俊鹏 and 赵J 微生物学报. (2006). 蛭弧菌的最新研究进展. 46:1028-1032.
6.国外医药:抗生素分册 顾J. (2020). 外排泵抑制剂研究进展. v.41:3-12.
7.Samuel ADT, TP Pitta, WS Ryu, PN Danese, ECW Leung and HC Berg. (1999). Flagellar determinants of bacterial sensitivity to chi-phage. Proceedings of the National Academy of Sciences of the United States of America 96:9863-9866.
8.Collier JJBebaGrm. (2019). Cell division control in Caulobacter crescentus. 1862:685-690.
作者|赵婧
审校|617
编辑|笑咲


