
美国营养协会定义个体化营养

之前我们曾报道过不少布局个体化营养的企业,包括雀巢、DSM 这样的巨头,也有 DayTwo、Baze、Viome 这样明星创业公司。
延伸阅读:
聚焦个体化营养,雀巢、DSM布局,多家创业企业融资 | 大事件
在这些公司的业务中,个体化营养或被视为一种针对某种慢性疾病的饮食干预措施,比如 DayTwo 对糖尿病患者的饮食管理;或是根据用户问卷和生理指标提供不同的膳食补充剂组合,比如 DSM 的膳食补充剂定制业务。
美国营养协会(ANA)12 月 19 日发表文章对“个体化营养”进行了明确定义:个体化营养(PN)是利用人的个体特征来实施营养,从而达到预防、管理、治疗疾病和优化健康的一种策略。
该文章发表在 Journal of The American College of Nutrition 上,由 ANA 联合塔夫茨大学、多伦多大学、美国西部州立大学、马里兰综合健康大学等多个研究机构的专家共同发布。
文章指出:“基于多学科领域的先驱者们所做的开创性工作,这一定义可以作为一个起点,将个体化营养嵌入医疗系统来预防、治疗和管理疾病,优化人类健康。”

ANA 以推动个体化营养为使命,该组织认为个体化营养被充分认识、利用和发展的前提是需要明确的定义。ANA 将在此定义的基础上,为个体化营养的实践制定强有力的标准。
文章指出了推动个体化营养发展的三个要点:PN 科学和数据、PN 专业教育和培训、PN 指导和治疗,并在文中对这三个方面进行了具体阐述。
PN 科学和数据:这是建立在观察性研究、随机对照试验、“公民科学计划”或众包项目数据所获得的知识和理解的基础上的。
文章写道:“新兴和先进的组学技术也有助于建立强大的 PN 知识库,方法和技术的结合能够更好地理解营养干预对个体和群体的潜在影响。”
PN 专业教育和培训:这是将传统的临床护理概念与先进的 PN 干预相结合,以促进健康和疾病管理。
文章写道:“PN 的临床应用要求从业者须接受充分的培训,以便在实践中应用这些知识。应针对不同的医护专业人员进行相应的专业教育和培训。”
PN 指导和治疗:这是指临床方法,以客户或患者为中心,以制定有意义的个体化营养建议。
文章写道:“在 PN 范式中,健康和疾病不是二元的,而是存在于一个连续变化的统一系统中,这个系统不是孤立的,而是相互联系的。PN 从业者需要描绘出这个系统和功能中最重要的联系,以便更充分地了解个体的表型和相应的营养需求,并给出有效的建议。”
ANA 认为,个体化营养是人类健康的核心,但如果要把它变成医疗保健的核心,就必须激发它的巨大潜力。与任何新兴学科一样,个体化营养必须进一步发展,才能成为一门被认可、受人尊重和可扩展的学科。
ANA 营养科学与教育主管 Corinne Bush 博士表示,基于个体独特的基因组、微生物组、生物化学指标等的个体化营养干预措施,在抵御慢性疾病和促进健康方面具有深远的潜力。
因此,ANA 召集专家起草了这份“个体化营养”的定义,作为倡导和推动个体化营养发展工作的一部分,该机构希望更多的营养科学家能够在这个层面达成共识。这代表着 PN 领域的一个飞跃——定义该术语及其范畴是将其嵌入医疗体系核心的关键一步。
ANA 认为,这一定义将在研究、数据、培训、产品、服务和临床实践中促进PN标准化和可扩展性,并有利于推动相关优惠政策。
本节资料来源:
https://doi.org/10.1080/07315724.2019.1685332
https://www.nutraingredients-usa.com/Article/2019/12/23/A-leap-forward-ANA-proposes-definition-for-Personalized-Nutrition
AI帮你找到功能食品的好口味

众所周知,除了维生素 C,大多数功能性成分的味道并不是很好,这是开发功能性食品和饮料的一个常见痛点。某种程度上来说,口感和味觉永远排在食品饮料的头等重要位置。
美国 Analytical Flavor Systems(AFS)公司专门开发了一个人工智能平台——Gastrograph AI,通过深度学习来自于消费者的感官数据集,模拟人类对味道、香气和质地的感知,并用来预测消费者对食品和饮料的偏好。
该平台旨在帮助快消品企业为目标消费群体建模、理解和优化产品的味道、香气和口感,开发符合消费者口味预期的新产品,或者优化现有产品以满足特定目标消费者群体,并进入新市场。
有了 AFS 的 Gastrograph AI 平台,产品开发人员不再需要为某一产品的口味进行一轮轮的几天或几周的测试和调配,AI 可以快速预测哪些口味消费者会喜欢,以及它与市场上其他同类产品的比较。
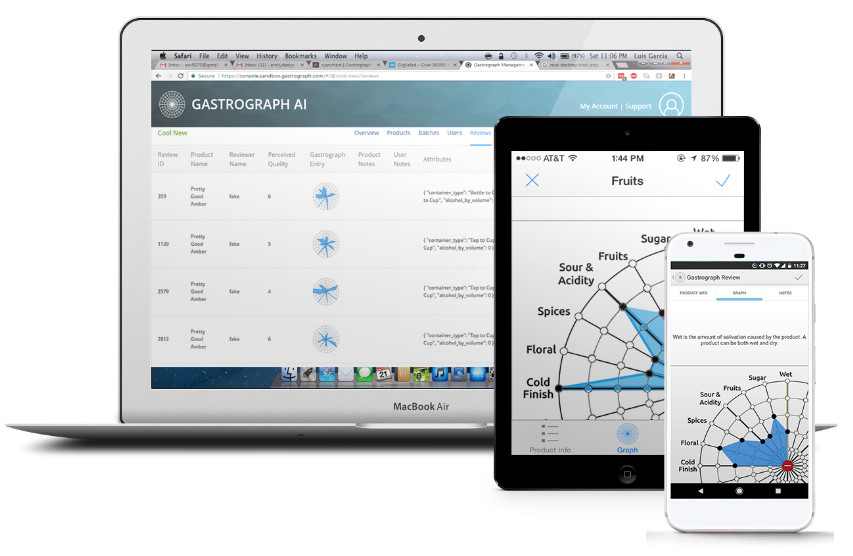
Gastrograph AI 平台的产品测试面板
据介绍,该公司已经收集了来自美国各大城市以及全球重点城市的感官数据集。这些数据来自设在各个城市的常设委员会,他们会品尝市场上任何一种新的、有趣的产品。
拥有如此广泛的消费者反馈数据集,使得 AFS 甚至能够预测各个城市和人口层面的口味偏好。现在,他们可以准确预测世界各地的目标消费者会对测试产品有什么口味感受,以及他们会有多喜欢,并从中选出消费者体验好的测试产品。
然后该平台把预测结果与一堆竞争者进行对比,进行全面的探索性搜索,找出三到四种市场上不存在的、没有直接竞争对手的、预计更受欢迎的潜在口味。
它还能给出原料配比公式,主动屏蔽功能成分的味道。以能量饮料为例,该公司可以通过其 Gastrograph 平台运行一个能量饮料配置文件,以确定哪些成分可以调整,以开发一个首选的口味配置文件。
目前,该公司已为美国、法国、荷兰、英国、中国和日本的近 30 家食品饮料公司推出了多个成功的产品,几乎所有产品的表现都超出了预期。
在去年完成 A 轮 400 万美金的融资后,该公司已于今年在上海开设了新的全球办事处。
本节资料来源:
https://www.gastrograph.com
https://www.nutraingredients-usa.com
GaRP与药物联合治疗IBS和IBD可降低药物副作用

2019年12月19日,Anatara Lifesciences 公司宣布完成 GaRP 膳食补充剂针对肠易激综合征(IBS)的临床试验方案,目前正在选择临床研究组织(CRO),并将于 2020 年第二季度启动临床试验。
GaRP 是 Anatara 公司专门针对炎症性肠病(IBD)和肠易激综合征(IBS)这两类肠道慢性疾病,开发的一种靶向肠道菌群的多成分膳食补充剂。
根据今年 10 月 14 日该公司发布的 GaRP 临床前研究数据,GaRP 与这两种肠道疾病的常用治疗药物联合使用,对减轻炎症有辅助作用,并有减少治疗药物剂量的潜力,这就意味着或能降低这些药物的破坏性副作用(如败血症),该作用已在 IBD 动物模型中得到证实。
研究表明,GaRP 有潜力广泛用于各种慢性胃肠道疾病的辅助治疗。该公司明确将该产品定位为辅助作用,也就是说不会干扰常用的胃肠道疾病处方药,以及其他常用的补充和替代药物,如益生菌的有效性。而关于这一点,Anatara 已经利用体外肠道模型证明,GaRP 并不影响益生菌的吸收及潜在活性。
Anatara 的首席执行官 Steven Lydeamore 先生说:“这些数据为 GaRP 有潜力改变游戏规则提供了强有力的科学证据。该产品的活性是由于其独特的配方,而且膳食补充剂不需要经过传统的、正式的药物审批途径,能够高效地开展临床研究。”
肠易激综合征是最常见的胃肠道疾病,影响全球约 11%的人口,而 IBD 影响全球约 500 万人。
目前的药物治疗有很高的失败率和严重的副作用,超过 50%的 IBD 患者尝试过控制疾病的补充和替代药物(CAMs)。资料显示,2018 年,仅美国用于胃肠道补充剂和非处方(OTC)药物的支出就达 80 亿美元。Anatara 正是看中了这一巨大的医疗需求和市场机会。
本节资料来源:www.anataralifesciences.com
武田Entyvio皮下注射剂型未获FDA批准

武田制药(Takeda)12月20日消息,美国 FDA 已针对该公司提交的皮下注射剂型 Entyvio(维多珠单抗)的许可申请(BLA)发布了回应函(CRL)。FDA 的回应函显示, Entyvio 皮下注射制剂(SC)作为针对中重度溃疡性结肠炎(UC)患者的维持疗法,在美国的申请未获批。
武田正在评估 CRL的细节,收集解决 FDA 问题所需的信息,并将进一步与 FDA 密切合作,以期 Entyvio SC 制剂在美获得批准。
目前,Entyvio SC 制剂治疗中重度溃疡性结肠炎(UC)和克罗恩病(CD)患者的营销授权申请(MAA)也正在接受欧洲药品管理局(EMA)的审查。在美国和欧盟,BLA 和 MAA 申请还包括 Entyvio SC 制剂的预充式注射器和注射笔,额外的给药方式将为患者提供更多的选择。
如果获批,Entyvio 将成为唯一一种针对 UC 和 CD 可同时提供静脉输注剂型(IV)和皮下注射剂型(SC)产品的维持疗法。
Entyvio IV 制剂早在 2014 年即获得 FDA 批准用于治疗中重度 UC 和 CD 患者,并已在全球 60 多个国家获准上市销售。在美国,已有超过 15 万名患者使用了 Entyvio IV 制剂。
武田坚信 Entyvio SC 制剂能给中重度 UC 患者带来潜在的好处,期待最终能够将这一重要的给药方式带给维持治疗的患者。
延伸阅读:
UEGW:武田发布IBD真实世界研究结果,维多珠继续罕逢敌手!
本节资料来源:
https://www.takeda.com/newsroom/newsreleases/
韩国 UC 新药在中国获批临床
韩国制药公司 Bridge 12 月 26 日宣布,中国国家药品监督管理局(NMPA)药品评审中心(CDE)批准了该公司于2019年9月25日提交的 BBT-401 实验性新药(IND)申请,该候选药物是一种强效的治疗溃疡性结肠炎(UC)的 Pellino-1 抑制剂。
Bridge 计划于 2020 年 5 月启动针对中国受试者的 BBT-401 的Ⅰ期研究,该研究将以单次或多次递增口服剂量评估候选药物的安全性、耐受性和药代动力学特征,Ⅰ期研究预计于 2020 年底完成。
根据 2018 年 12 月签署的合作开发与许可协议,韩国大宇制药获得了 BBT-401 在中国、日本和韩国等 22 个亚洲国家的开发和商业化独家权利,而Bridge和大宇制药这两家公司一直在亚洲国家就 BBT-401 的临床开发进行密切合作。
BBT-401 是由韩国成均馆大学和韩国化学技术研究院发现的一种新型小分子 Pellino-1 抑制剂。该候选药物在美国开展的临床研究要早于亚洲,目前正在对美国活跃期 UC 患者进行 II 期临床研究。
Bridge 是一家成立于 2015 年的临床阶段生物技术公司,总部位于韩国,在美国和中国都设有分支机构。Bridge 专注于那些高度未被满足需求的治疗领域,如溃疡性结肠炎、纤维性疾病和癌症。
目前该公司在研产品除了 BBT-401,还包括 BBT- 877,这是一种 Autotaxin 抑制剂,用于治疗各种纤维化性间质性肺疾病,包括特发性肺纤维化(IPF),该候选药物已于2019年7月独家授权给德国勃林格殷格翰制药集团;针对非小细胞肺癌(NSCLC)的癌症治疗候选药物 BBT-176 也在开发中。
本节资料来源:www.firstwordpharma.com/node/1690169
Carbiotix 利用微生物组调节治疗平台开展神经炎症研究

Carbitix 公司 12 月 23 日宣布,该公司与意大利维罗纳大学医学系签署了一项合作协议,将在 2020 年利用 Carbitix 微生物组调节治疗(MMT)平台进行一项关于神经炎症领域的研究。
双方将重点研究短链脂肪酸或 Carbiotix 微生物组调节治疗(MMT)产生的代谢物对中性粒细胞功能调节作用的影响,以及这些细胞对神经炎症的贡献。
对于此项合作,Carbiotix 首席执行官 Kristofer Cook 评论道:“这是 Carbiotix 在不同适应症领域探索公司 MMT 平台潜力的首次学术合作。”
维罗纳大学的研究员 Elena Zenaro 博士在之前的研究中证实了特定代谢产物水平升高与神经炎症风险降低之间的关系。她说:“Carbiotix 的 MMT 平台关注的重点是提高关键代谢产物。在我自己的研究和最近亚洲的研究中,已经证实了肠道健康、关键代谢产物和神经炎症之间的联系,这表明 MMT 在治疗一系列神经退行性疾病方面可能具有未被开发的潜力。”
Carbiotix 是瑞典的一家开发微生物组调节疗法(MMT)的生物技术公司,该公司通过创新配方来促进肠道菌群的特定关键代谢物的产生,从而达到治疗不同的代谢和慢性疾病的效果。
目前该公司的在研治疗管线还包括高血氨症和炎症性肠病。
本节资料来源:www.carbiotix.com


