
首先非常感谢热心肠研究院的邀请,使我可以在《肠·道》这个舞台给大家分享我们的研究。我是来自深圳湾实验室的唐啸宇,今天演讲的题目是《人体微生物天然小分子》。

我们生活在充满微生物的世界,微生物无处不在。据统计,地球上微生物的数量远远大于我们可以看到的星辰。不管在土壤当中,还是在海水当中,我们都可以看见数以亿计的微生物。
微生物可以生活在非常极端的条件,比如说热泉当中,当然它们也存在于我们的身体里面和身体表面。
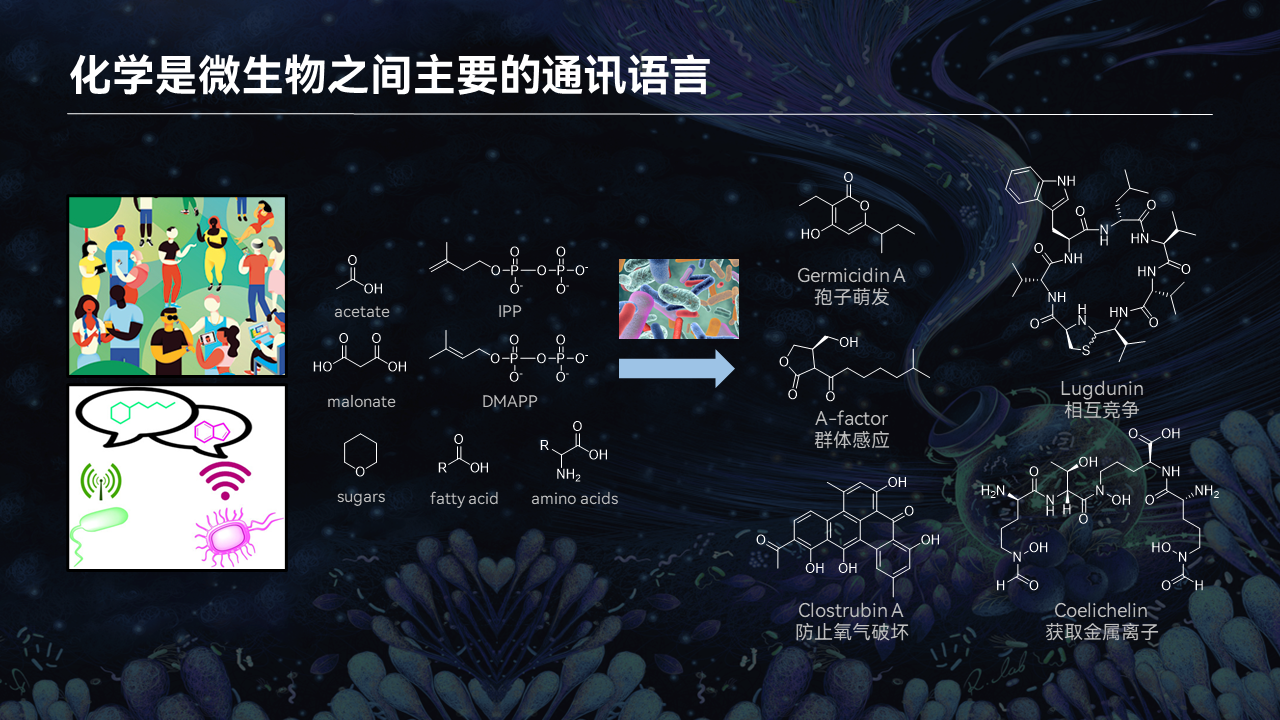
我们人之间通过语言和动作进行交流,那微生物通过什么进行交流呢?微生物其实主要通过化学小分子进行通讯交流。
微生物具有合成各种各样复杂天然小分子的能力,它们可以使用非常简单的底物进行合成。这些被合成的天然分子具有多种多样的活性,控制着微生物与外界的交流。
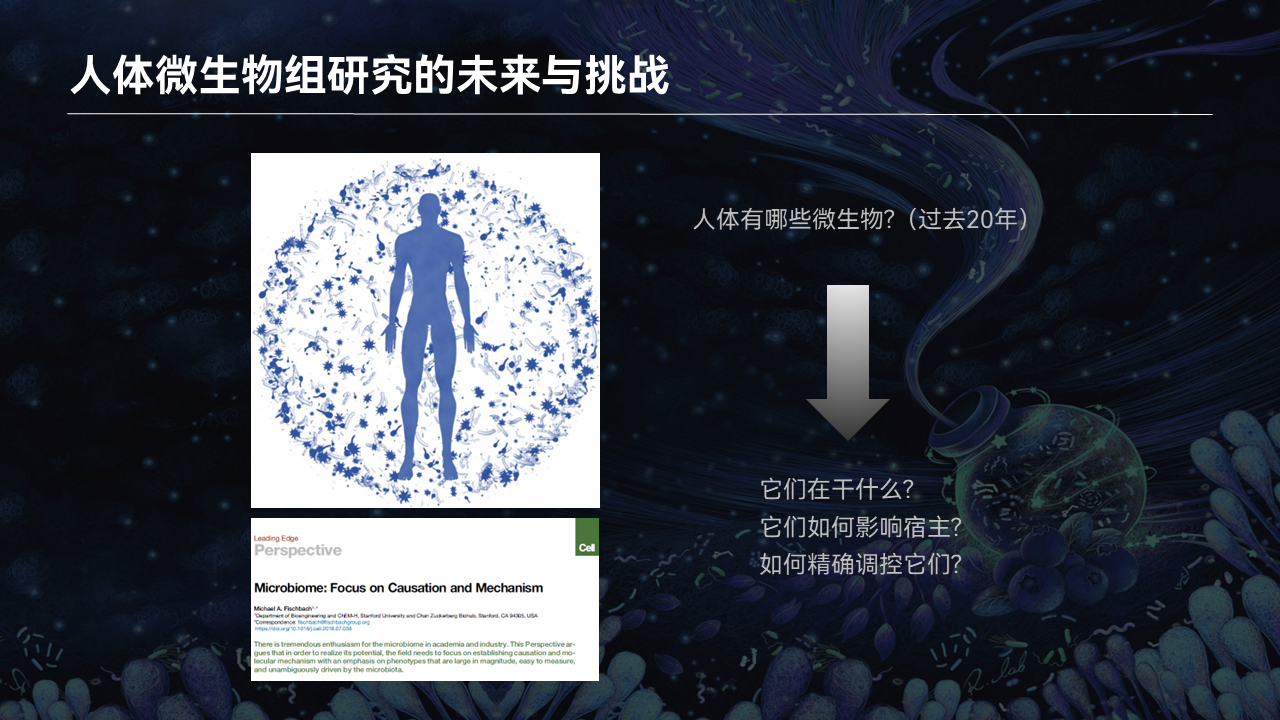
在过去的20年当中,通过测序技术的蓬勃发展,我们认识到人体当中还有大量的微生物。然而下一步微生物组的研究将往何处走呢?
在2018年的一篇综述当中,斯坦福大学的Michael Fischbach教授提出,我们微生物组的研究将更多地集中在机制的研究、机制的解析。我们需要知道微生物组在我们人体当中干什么,它们如何影响宿主的健康,我们通过什么样手段可以精确地调控它们。
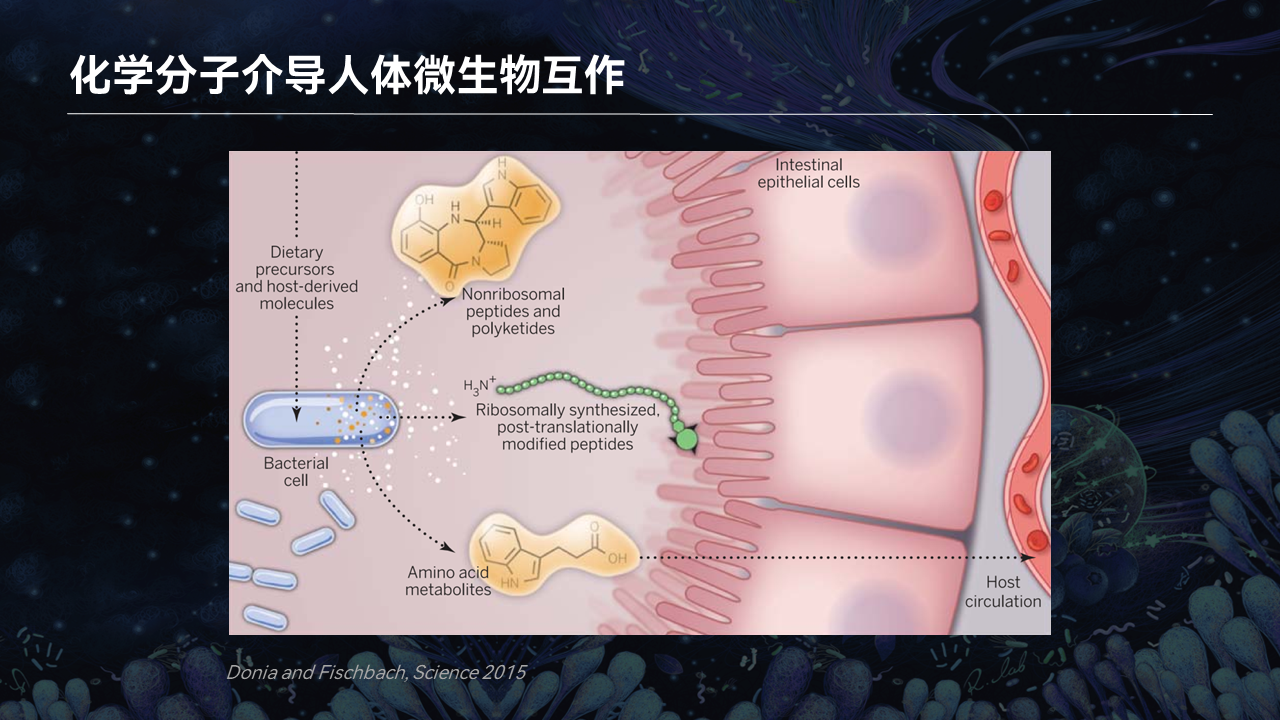
其中,化学分子介导微生物与人体互作成为研究的热点。
在这篇Science的综述当中,普林斯顿的Donia教授和斯坦福的Fischbach教授提出,人体微生物产生的小分子在影响人体健康当中发挥非常重要的作用。这些小分子可以进入我们的血液循环,影响人体的健康。
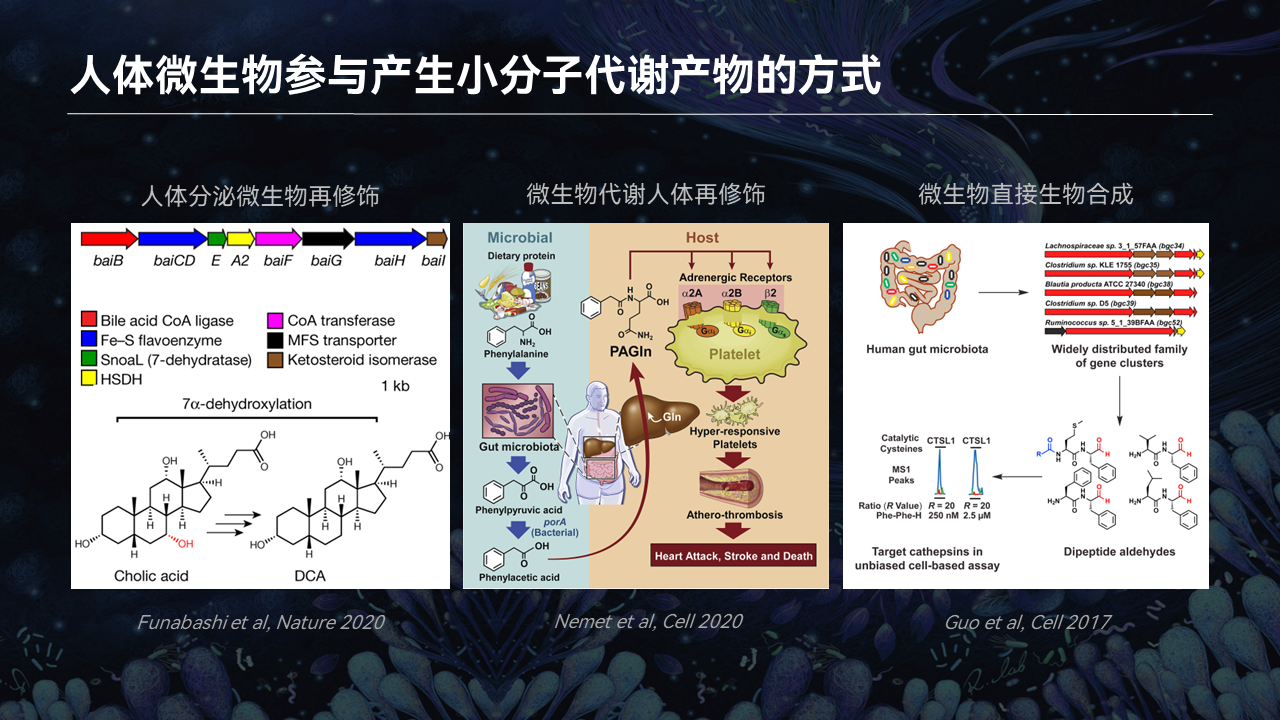
微生物是如何在人体当中产生小分子的呢?
这里可以归纳成为3种模式:第一种是人体产生了一些激素类的化合物,比如说胆酸,然后被肠道的小分子利用,产生次级胆酸,影响人体健康;
我们人类每天摄取大量的食物,微生物可以利用这些食物产生一些新的分子,然后再被体内代谢,通过协同作用产生一些新的分子影响人体健康。当然微生物也具有从头合成的能力,用简单的分子模块形成复杂的活性小分子。

在2014年,Michael Fischbach团队在Cell上面发表了一篇经典的文章,他们系统地分析了人体微生物当中所含有的可以合成天然小分子的生物合成基因簇。
这篇文章也被Nature杂志在2019年的回顾当中列为里程碑式的研究。

在这一项研究当中,Micheal和他的团队开发了新的算法,从JGI数据库当中分析人体微生物组可以产生天然小分子的生物合成基因簇。
他们发现,在人体微生物当中含有大量的可以产生天然产物、天然小分子的生物合成基因簇。随后他们通过一些化学手段发现,在生殖道当中的一株乳酸菌可以产生这样一个环肽分子,它具有非常特异性的杀灭病原菌的活性。
这提示我们,这些分子可以被利用作为药物,进行疾病的控制。
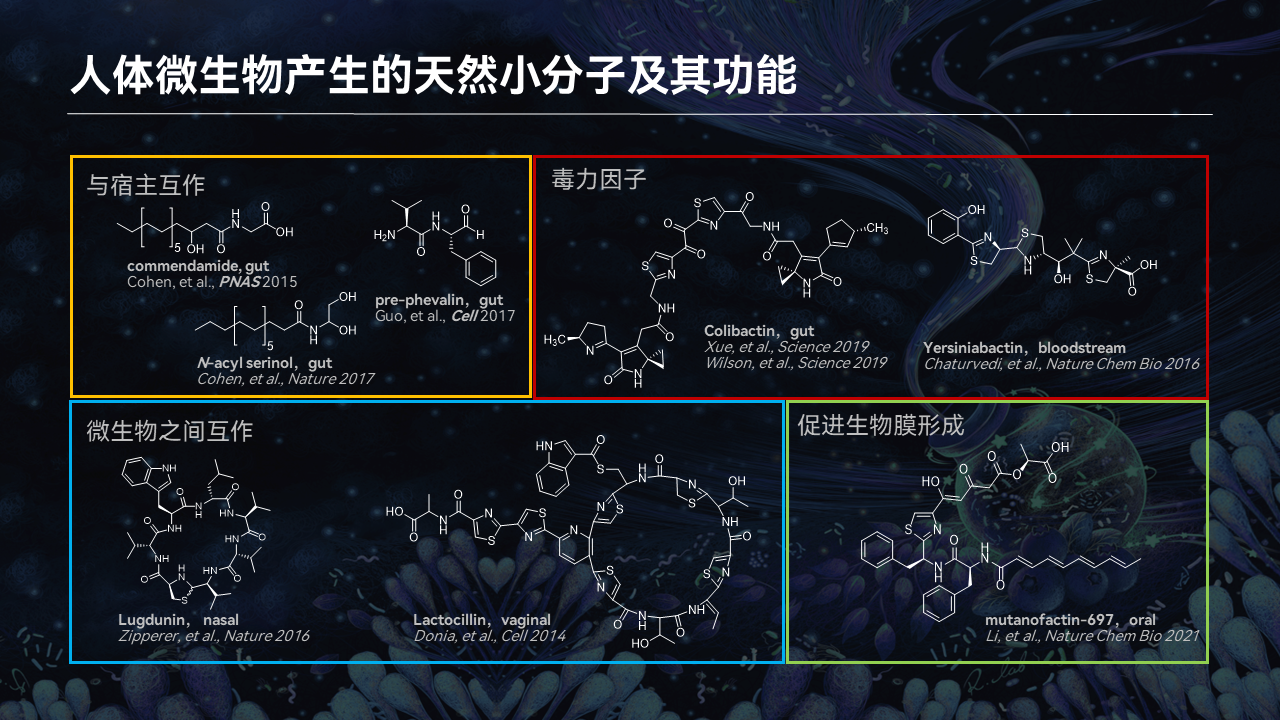
随着这项研究的发表,越来越多的人体微生物产生的小分子被发现。
这里有一些小分子参与宿主的互作,比如说调控蛋白耦联受体(GPCRG)、调控免疫细胞。有一些作为独立因子可以影响人类肠道的健康,比如说colibactin。它由大肠杆菌产生,可能与肠癌的发生相关。当然更多的是一些分子,它具有抗生素活性,可以影响微生物群落的发生和发展。当然有些分子被微生物体利用,产生生物膜。
在过去,更多的研究集中在肠道微生物产生的小分子,然而口腔微生物似乎被忽略了。
口腔微生物天然小分子
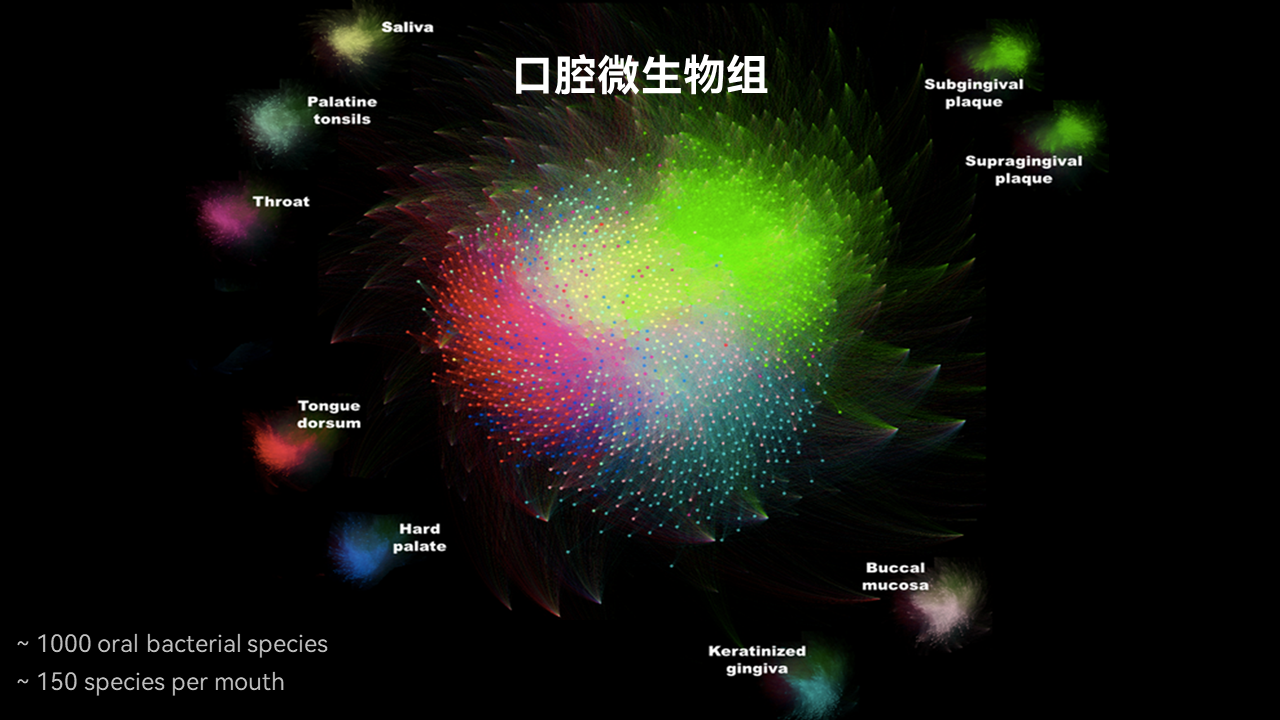
但我们知道,在口腔当中含有大量的微生物,其中每个口腔当中大约含有超过150个类型的微生物。

在先前的研究当中,已经证实口腔和肠道具有相同的合成天然小分子的能力。
在2019年,我们发表了一篇文章,系统分析了250个测序的口腔微生物。我们发现,这些口腔微生物含有超过4000个生物合成基因簇,可以用于天然小分子的合成,其中有一大半都是未知的。我们还发现,在口腔当中具有大量的小分子还未被鉴定。
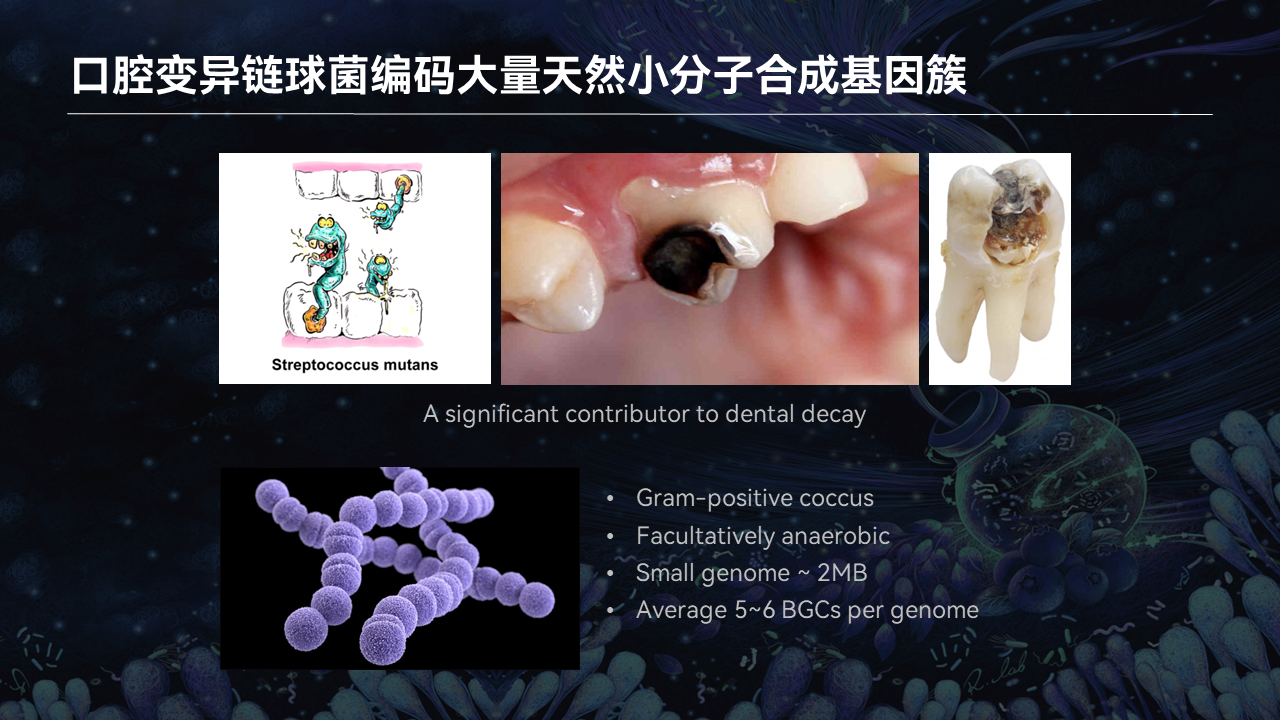
我们把目光首先集中在口腔变异链球菌。
它是口腔当中非常有名的一类微生物,可以导致龋齿的产生。而且这类微生物有非常小的基因组,它可以在有氧、无氧条件下生长,每个基因组上面含有5个左右的生物合成基因簇。
我们在想,这些生物合成基因簇可以合成什么分子?它是否参与龋齿的过程?
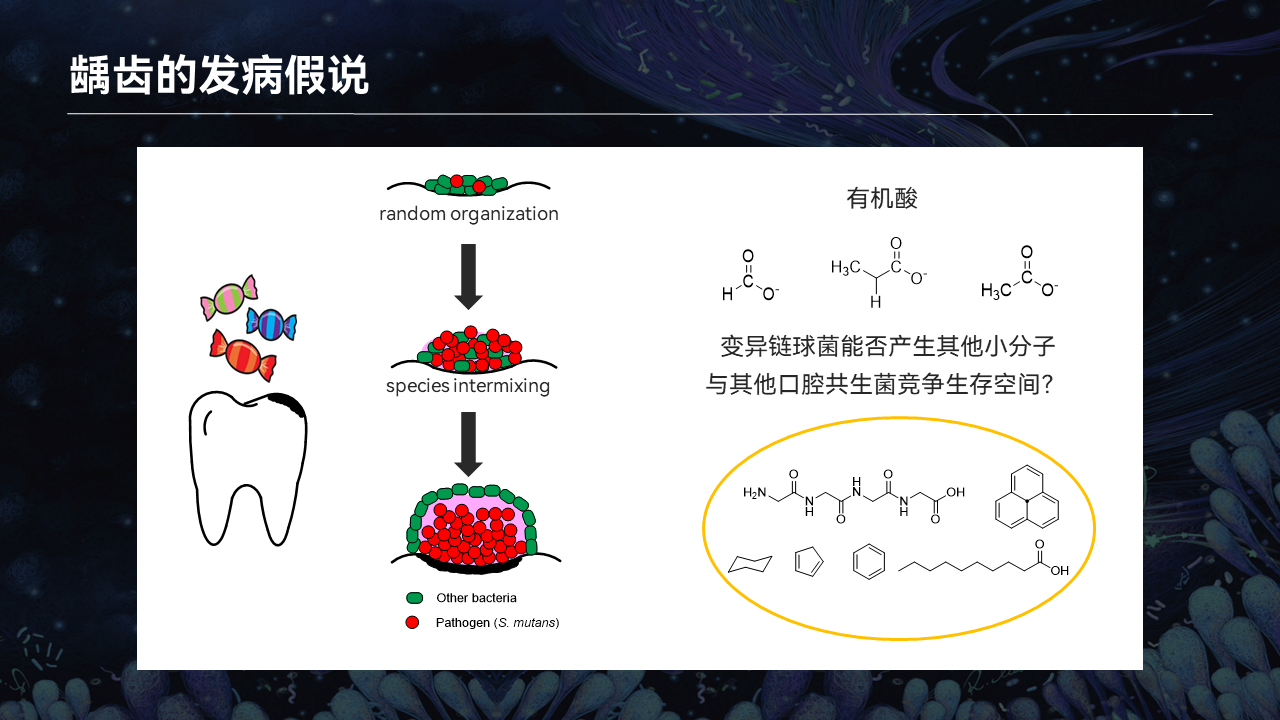
下面我们来看一下龋齿发展的假说。
在正常的口腔当中,变异链球菌和其他正常的微生物共生。当你消耗太多的糖以后,变异链球菌特别喜欢利用糖类产生有机酸分子,然后用有机酸分子去占领生态位,形成生物膜,然后就会一步一步地损坏你的牙齿。
我们当时的假设是:既然变异链球菌具有合成各种小分子的能力,它是否可以产生一些复杂的天然分子,在这种生态位的竞争当中发挥作用呢?
Reutericyclin(RTC)

首先,我们研究了变异链球菌当中的生物合成基因簇。
我们发现了有一株基因簇,它跟已经报道的一个抗生素基因簇非常的相似。这是一株从乳酸菌分离的基因簇,它可以产生一个叫reutericyclin的抗生素。我们在临床的样本当中发现,这株基因簇在龋齿患者的口腔当中有高表达。
然后,我们统计了这个基因簇和这个菌的全球分布。
我们发现,有许多临床样本当中分离到的变异链球菌都含有这个编码的基因簇。然后我们想知道这个基因簇能产生什么呢?是否能产生reutericyclin,简称为RTC这个分子,还是可以产生一些其他的分子。
我们首先做了菌株的敲除,把这个合成基因簇的关键基因敲除掉以后,进行了分析化学的研究。我们发现,这个基因簇可以产生4个分子,其中3个和已经报道的RTC非常的类似。我们还发现有1个分子,它失去了长链的脂肪酸。
所以说,口腔当中的变异链球菌同样存在产生可能的抗生素和其他分子的能力。
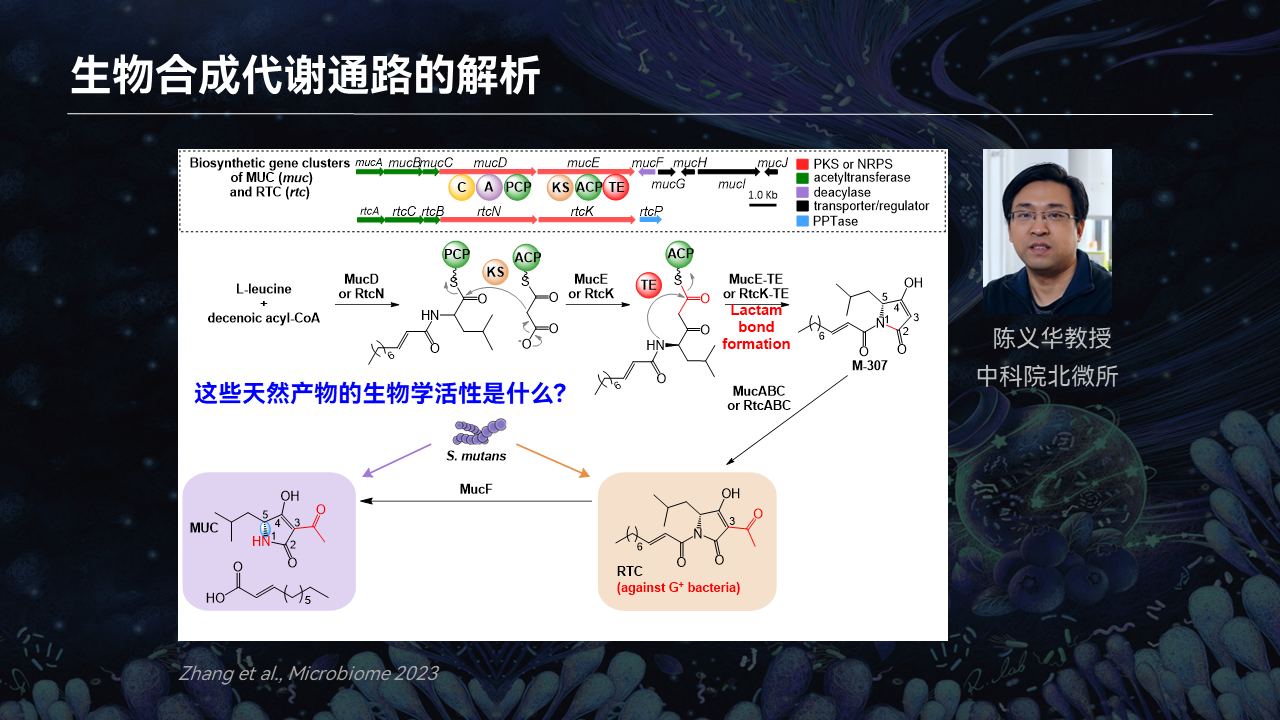
随后我们和中科院微生物研究所陈义华研究员团队合作,分析了它的生物合成,并在体外进行了重组。
我们发现,该细菌可以利用如氨基酸、脂肪酸一类非常简单的分子,合成RTC这个抗生素。它可以抑制许多革兰氏阳性菌,因为革兰氏阳性菌大量地存在于口腔当中。我们认为,这个分子可能会与这些微生物进行互作。
同时我们发现,在生物合成当中有一个MUC蛋白,它可以把脂肪酸切掉,形成MUC分子和中长链脂肪酸。
那这些分子的生物活性是什么?它的功能是什么?
我们首先研究了RTC,我们发现RTC具有优良的抗菌活性。
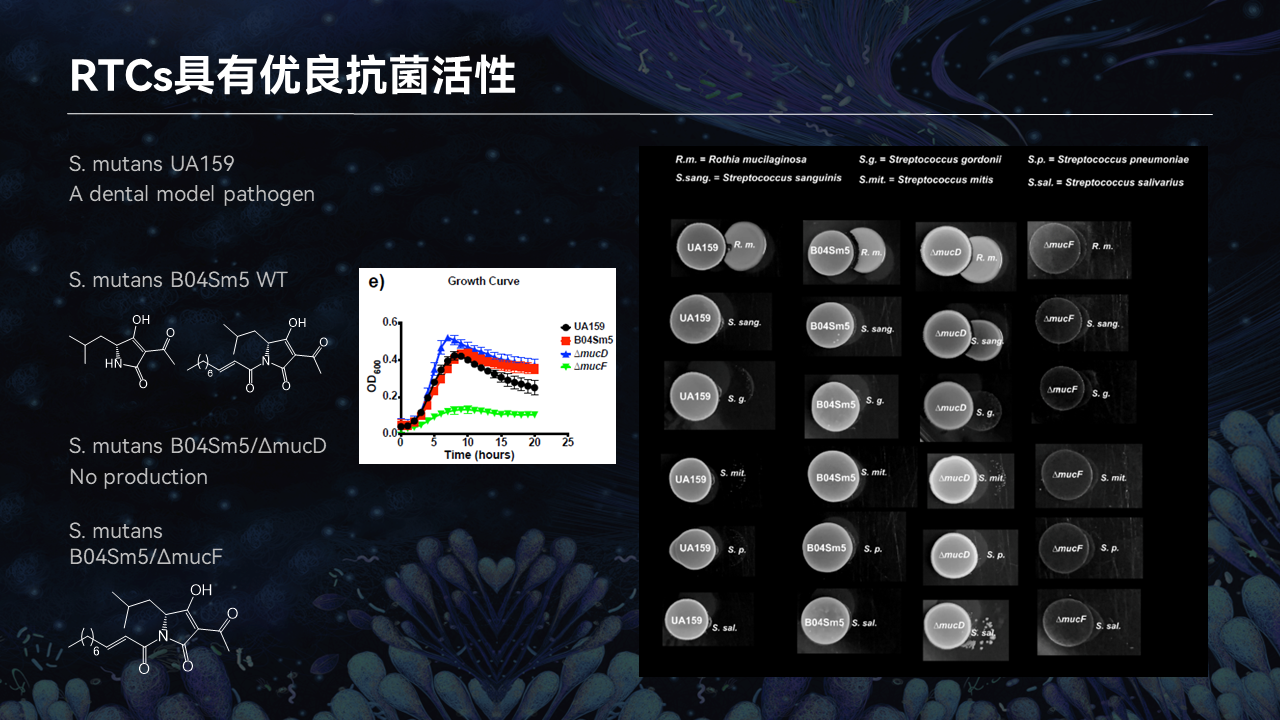
大家可以看到在这张PPT中,我们选取了4个菌株。第一个是变异链球菌UA159,它是一个研究龋齿的模式菌,不含有RTC这个生物合成基因簇。我们也有可以产生RTC和MUC的野生菌。我们也有敲除菌,它不能产生任何一个天然产物。当然我们也有F基因的敲除株,它只能产生RTC这个分子。
在平板的对抗实验当中,我们发现首先MUC这个对照菌,它可以产酸,因此可以去抑制其他的口腔正常菌。而野生菌含有RTC的这个微生物,它有更强的能力去抑制口腔当中其他的正常菌。
当我们把RTC这个基因簇敲除以后,它的能力大幅减弱。当我们只让它表达RTC这个分子的时候,它可以几乎杀死旁边所有的正常口腔微生物。
当然这里有个疑惑就是,RTC的产生菌是否也可以产生酸?

我们又做另外一个实验,在平板中加入缓冲液。大家可以看到UA159就失去了抑制正常口腔菌株的能力,只有具有RTC的菌株还保留着这样的能力,去杀死周围的正常口腔菌株。
当然我们又进一步地测试了RTC和MUC的活性。
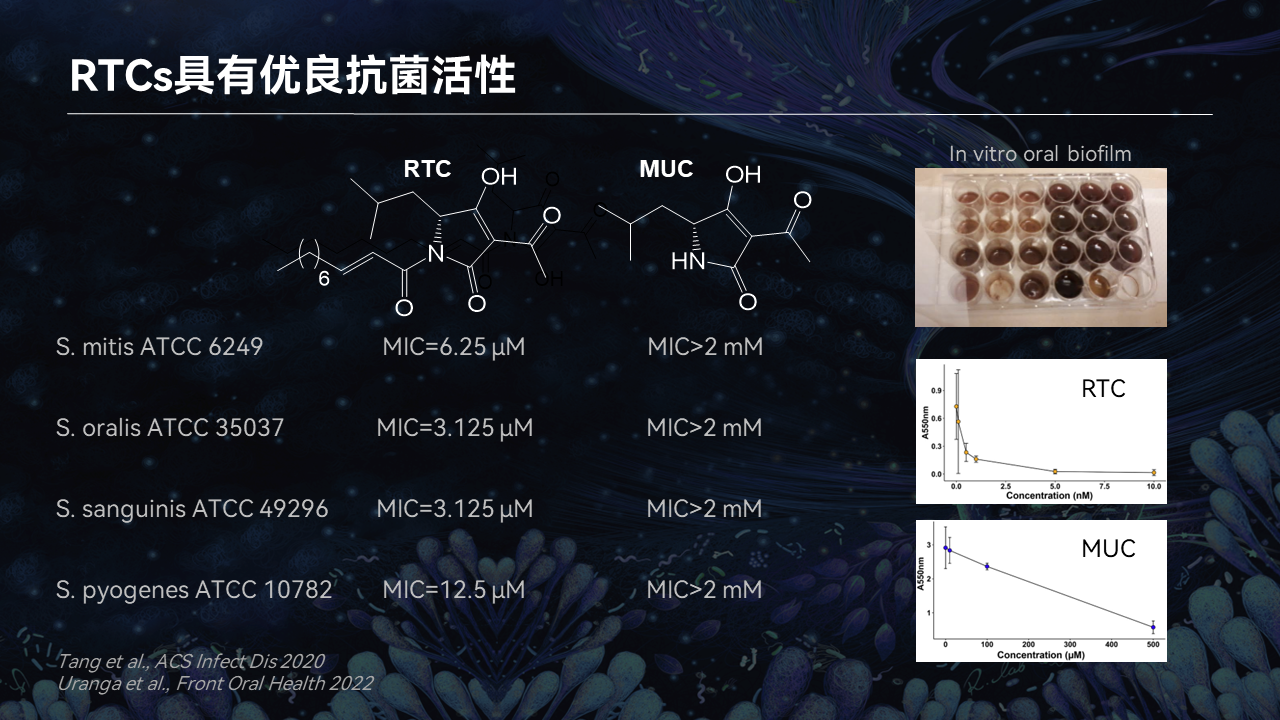
我们在测试当中选取了一些常用的口腔微生物,我们发现RTC具有非常良好的抗菌活性,可以抑制这些口腔当中的正常微生物,而MUC这个分子失去了这样的能力。随后我们构建了体外生物膜模型,我们选用口腔里采集的唾液,然后在体外重构生物膜。
当我们在生物膜当中加入了RTC这个分子,我们发现生物膜并不能形成。特别是在纳摩尔水平,就可以抑制口腔当中正常菌株生物膜的合成。但加入了MUC,尽管我们提高了非常高的浓度,它始终不能抑制生物膜的形成。
这进一步证明了,RTC可以帮助变异链球菌在口腔当中与正常细菌进行竞争。
MUC
当然我们对MUC这个分子的活性同样存在好奇,它到底发生什么样的作用呢?
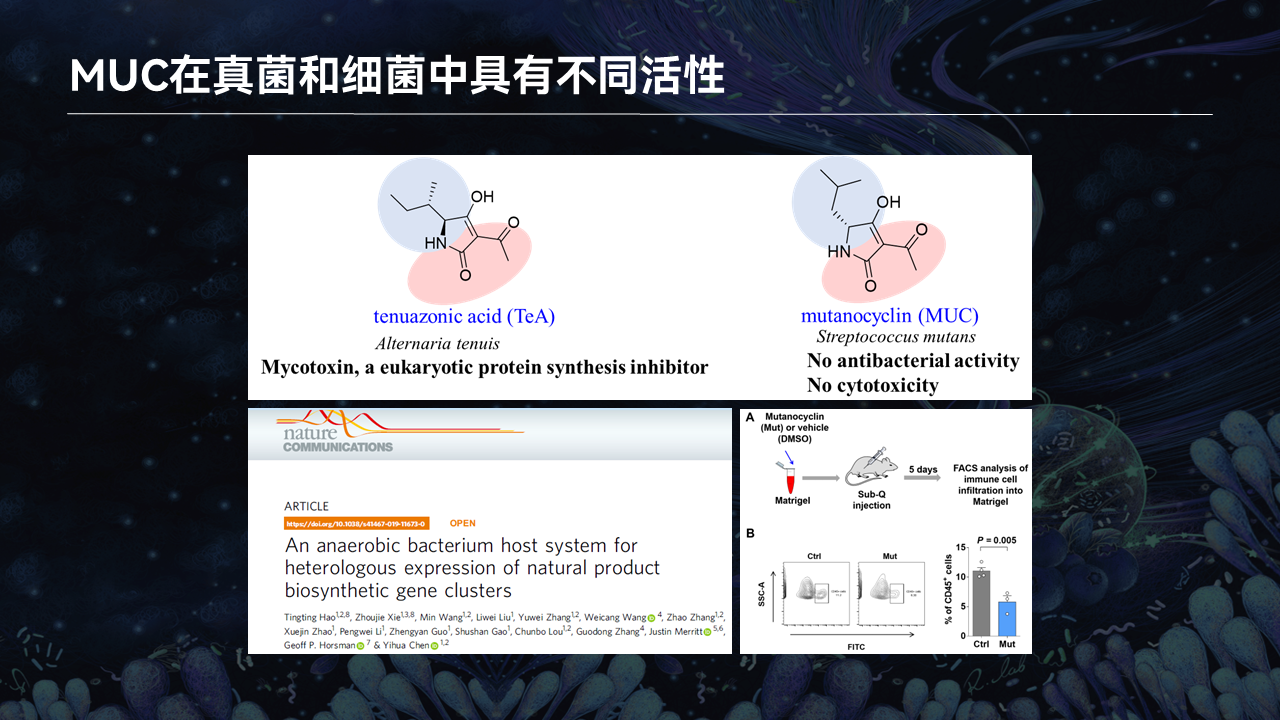
因为这一类的分子已经在真菌当中报道过,虽然它们结构上有一点点不同,但是这一类分子在真菌当中可能抑制真核生物的蛋白质表达。而在我们的测试当中,并没有发现MUC有任何的活性,没有抗菌活性,没有生物毒性。
在2019年发表的一篇文章当中,陈英华团队利用老鼠模型发现,MUC这个分子可能会影响人体的免疫,可以影响人体当中免疫细胞的表达。
是否这个分子可以帮助变异链球菌更好地定植在口腔当中呢?这个需要进一步的研究。

随后他们在另一项研究中发现,MUC这个分子具有抗真菌菌丝体生长的活性。
在体外的实验表明,加入MUC可以抑制口腔白色念珠菌的菌丝体生长。在老鼠模型当中,他们观测到了同样的现象,在加入MUC这个分子以后,白色念珠菌就不能产生菌丝体了。
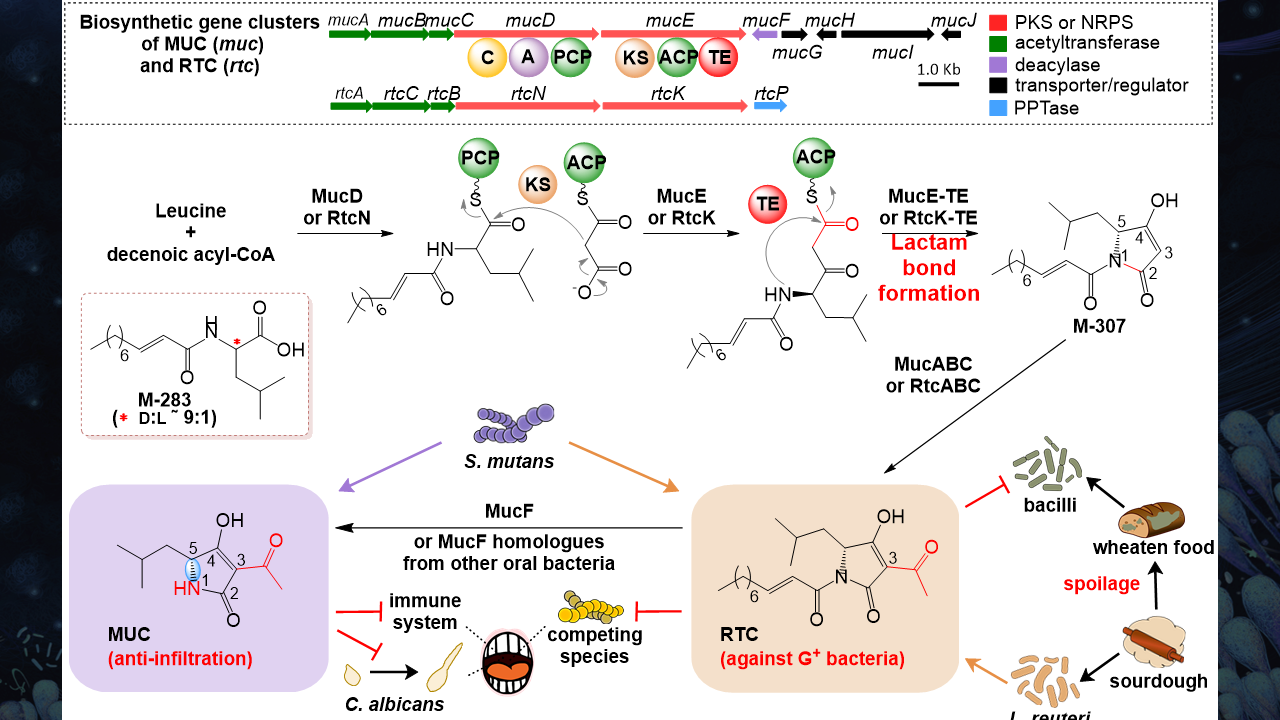
总结来说,我们在口腔变异链球菌发现了一组生物合成基因簇,通过这株生物合成基因簇,可以利用非常简单的氨基酸和脂肪酸类的小分子,产生RTC这样一个具有抗革兰氏阳性菌活性的天然分子。
当然变异链球菌可以通过MucF这个蛋白,把脂肪链切除以后只产生MUC这个分子,可能利用这个分子与宿主和真菌进行互作。
MUC这个分子也在面包工业被发现。在德国的面包房里面,人们分离到了乳酸菌株可以产生RTC,并且发现RTC对于发酵液的污染控制非常有效。
MUC vs RTC
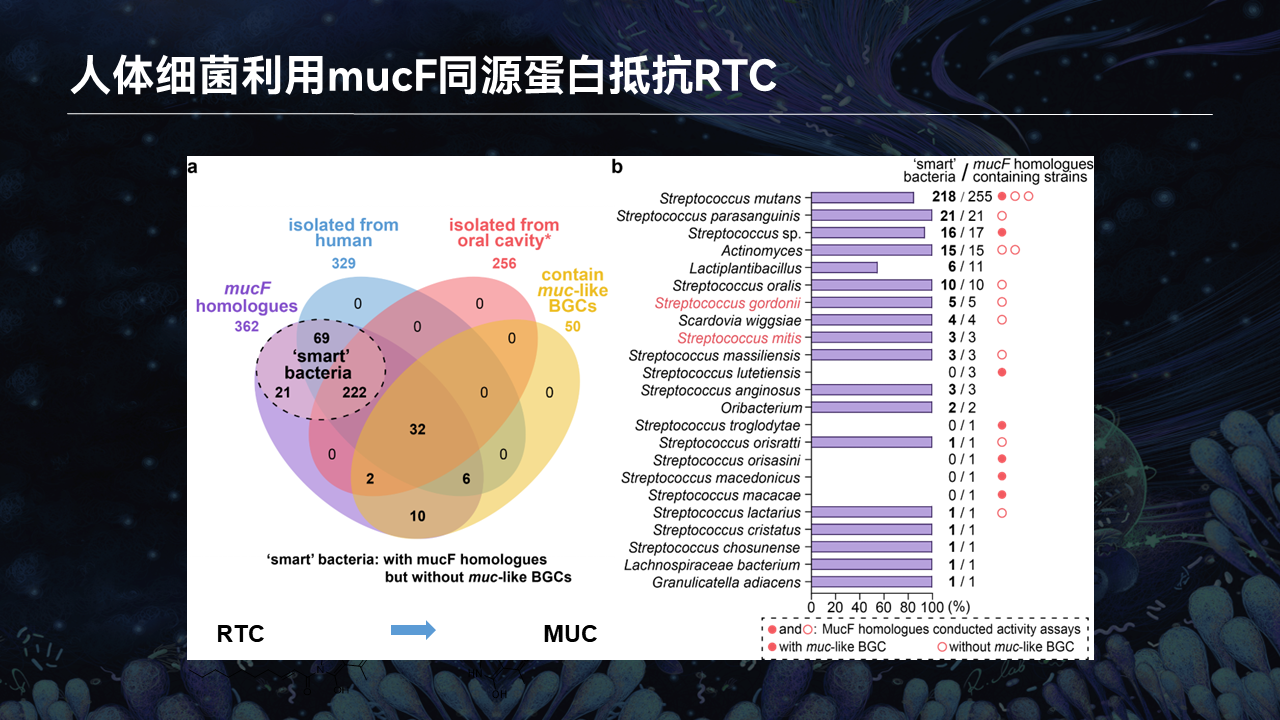
我们同时发现,MUC这个蛋白不光存在于变异链球菌,这株细菌在口腔中,乃至一些肠道菌当中也存在于MUC的同源蛋白。就是说可能生活在同样环境的微生物,它吸取了这个蛋白并利用了蛋白。
可能的原因是因为变异链球菌产生了RTC这个分子,它可以抑制其他的微生物,其他的微生物就需要利用这个蛋白,把RTC转变为MUC为我所用,用于其他的功能。
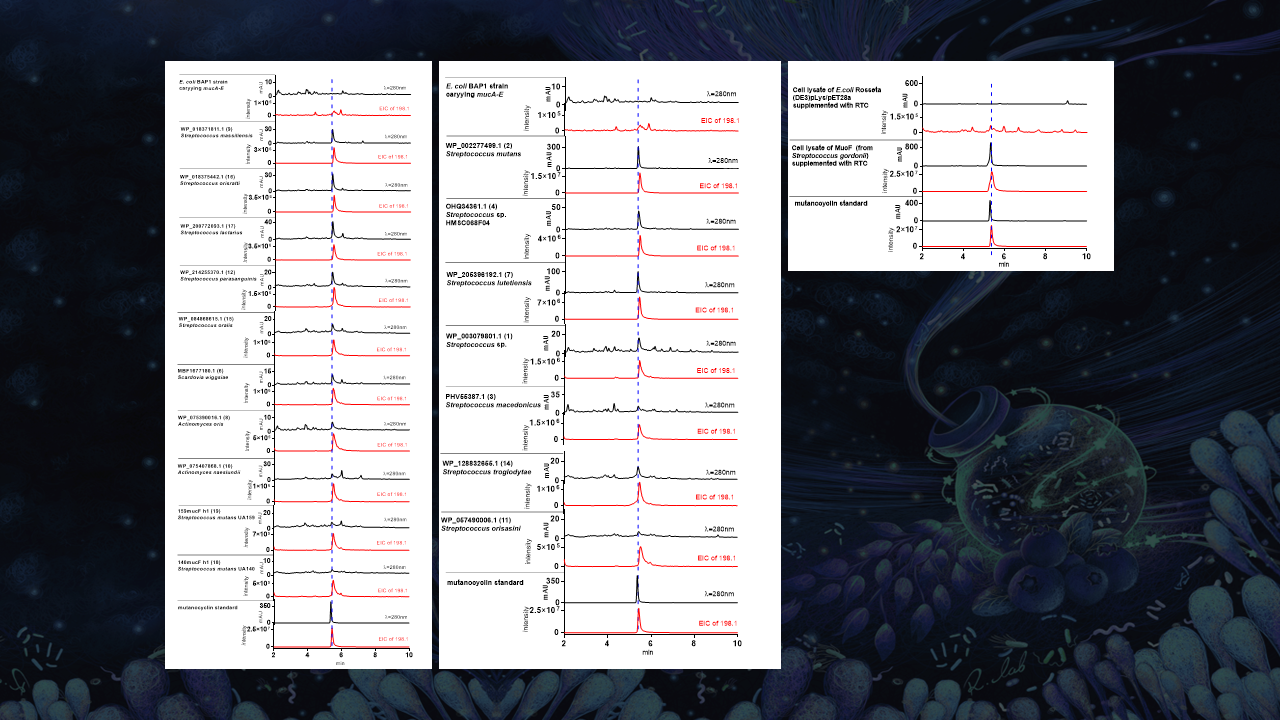
为了验证这个假说,我们选取了20多个口腔和肠道当中细菌编码的MUC同源蛋白,进行了体外表达并发现,这些分子、这些表达的蛋白可以将RTC这个分子转化为MUC这个分子。
这就证明了,在口腔包括在肠道当中,有很多的细菌可以将变异链球菌产生的RTC转化成MUC。但具体它们将把MUC做何作用,我们还未知。
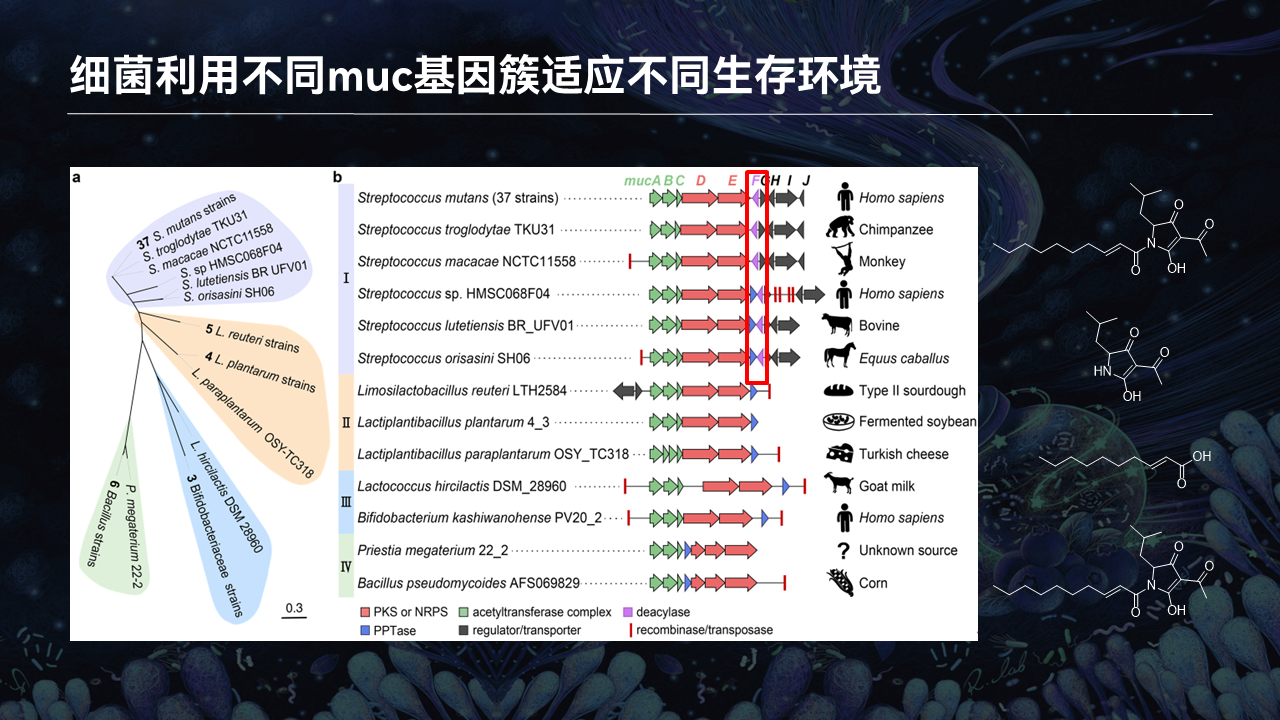
随后我们发现,其实有不同的细菌、共生细菌或者在体外的细菌都含有MUC这个生物合成基因簇。
其中非常有意思的发现就是,在共生环境中,不管是在人、动物、猩猩或者马发现的微生物,如果含有MUC这个生物合成基因簇,它们都含有MucF蛋白。这个蛋白可以切除长链脂肪酸,形成MUC和中链脂肪酸。
但在其他环境当中,非共生的环境当中发现的一些微生物,它失去了MUC这个蛋白。是否这些微生物只能产生RTC这个分子,用于与环境当中其他共生的微生物或者细菌进行竞争作用,以竞争获得生态位以获得更多的资源呢?这都需要进一步的研究。
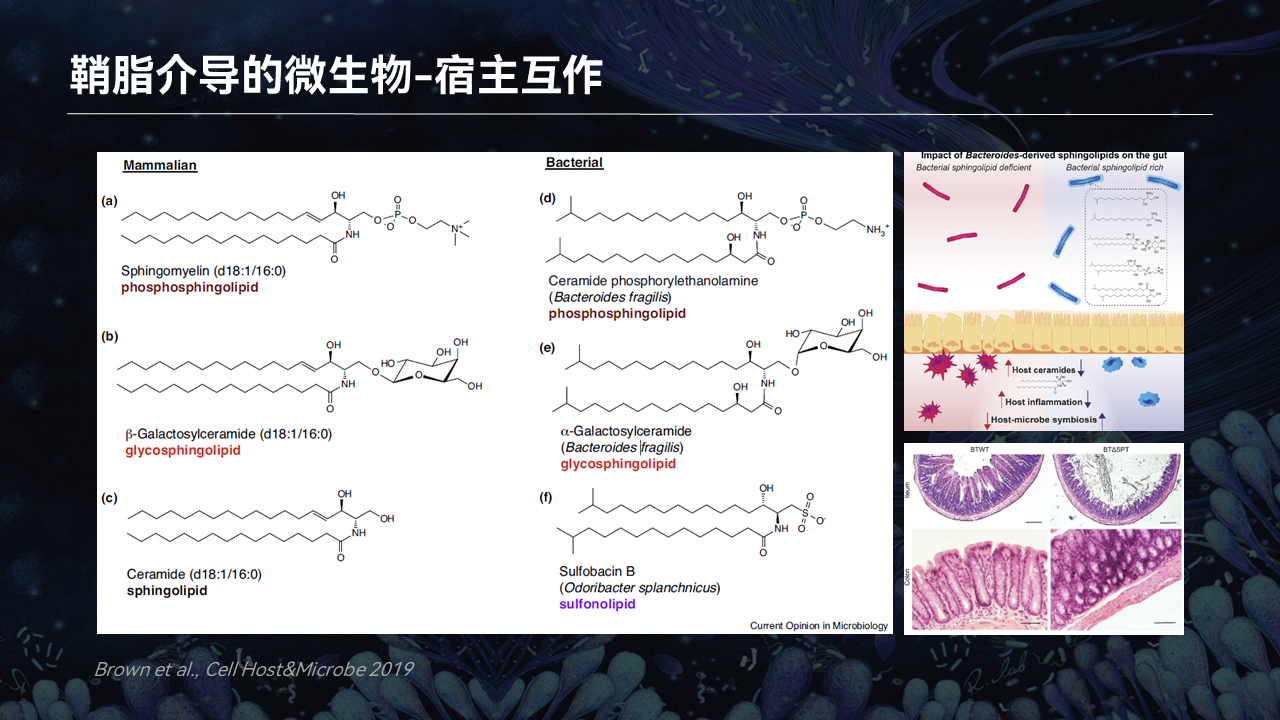
我们的课题组同样关注另一类分子——鞘脂类分子。
鞘脂类分子最早发现于人的脑部,当然也可以在各种各样的真核生物生物膜当中发现。在最近的研究当中,人们发现越来越多共生微生物,它们同样有产生鞘脂类分子的能力,当然它们的结构与人体产生的略有不同。
其中在一项研究当中,人们发现如果把拟杆菌的鞘脂合成基因进行敲除,拟杆菌就会破坏肠道、产生炎症。
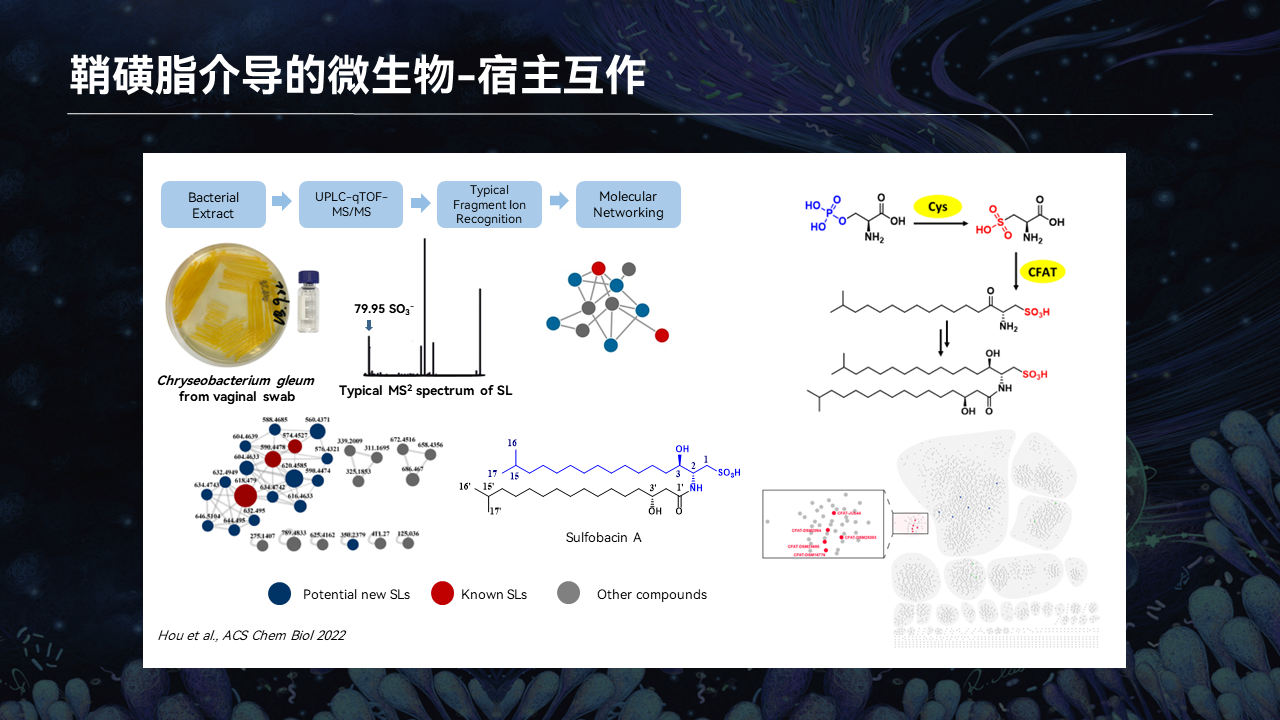
在最新的一项研究当中,我们发现从生殖道当中分离到的黄杆菌,具有产生一类鞘磺脂的能力。
随后,我们鉴定了产生鞘磺脂的基因。通过生物信息的分析,我们发现不光在生殖道当中,在肠道当中也存在着基因合成鞘磺脂。
鞘磺脂到底有什么样的作用呢?
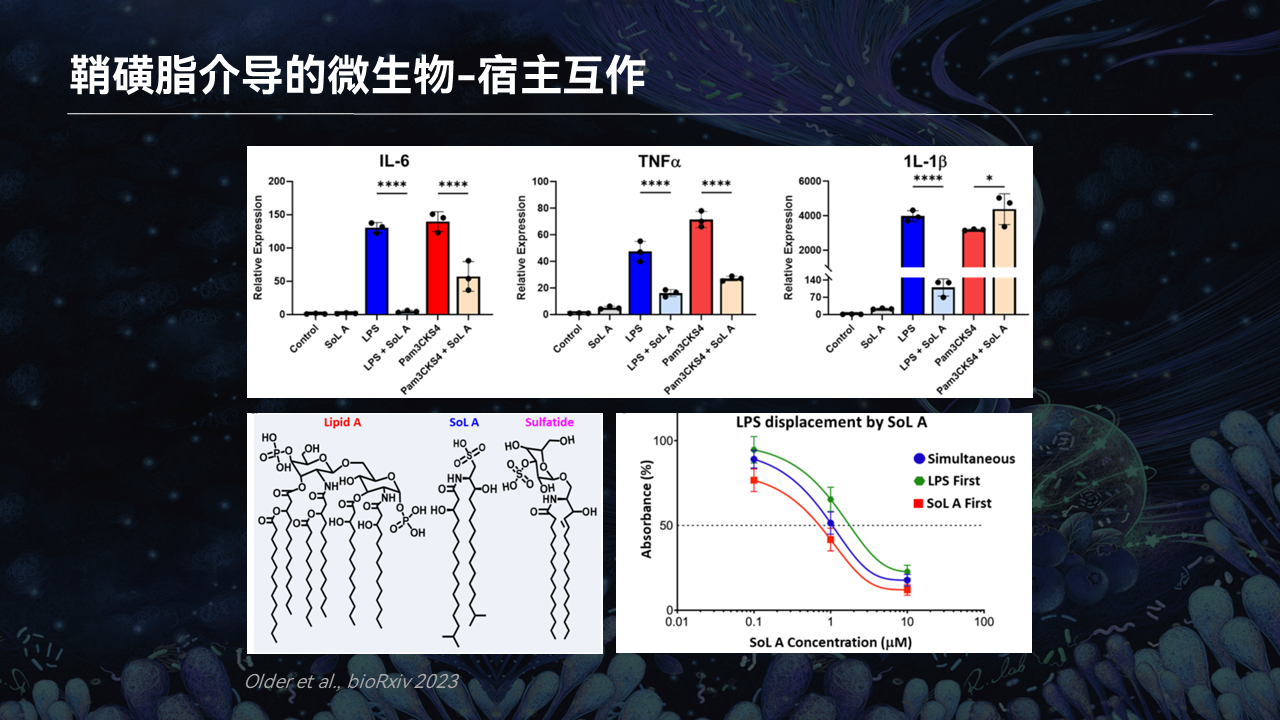
在最新的一个发表在bioRxiv的研究当中,研究者发现鞘磺脂可以和脂多糖(LPS)竞争抑制LPS的受体,从而抑制免疫反应的发生。
当然这只是非常初步的研究,需要进一步的更多的实验去证实这样的研究。
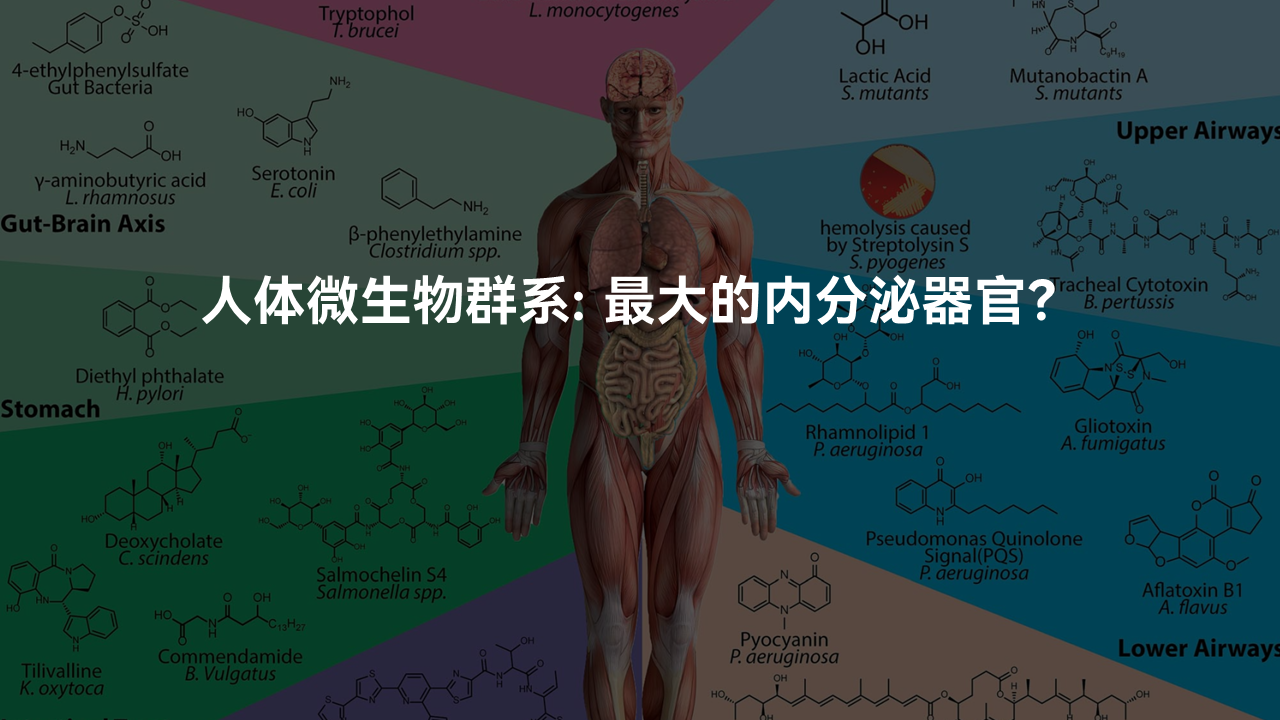
所以说人体当中的微生物其实可以被称为一个最大的内分泌器官,它与人体进行化学互作交换,产生大量的小分子代谢产物,影响人体的健康。
这里我们就需要更多的化学家、生化学家和分析化学家加入到人体微生物组的研究,与生物学家、微生物学家以及临床医学家合作,去探究人体微生物产生的天然产物、小分子代谢产物,以揭秘肠道微生物或者人体微生物与人类互作的分子机理。

最后,感谢大家聆听!


